Meticilina
 | |
 | |
| Datos clínicos | |
|---|---|
| Vías de administración | IV |
| Código ATC | |
| Datos farmacocinéticos | |
| Biodisponibilidad | No se absorbe por vía oral |
| Metabolismo | hepática, 20–40% |
| Vida media de eliminación | 25–60 minutos |
| Excreción | renal |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.000.460 |
| Datos químicos y físicos | |
| Fórmula | C17H20N2O6S |
| Masa molar | 380,42 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
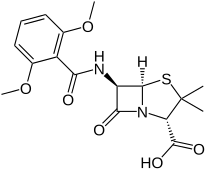
La meticilina ( USAN ), también conocida como meticilina ( DCI ), es un antibiótico β-lactámico de espectro estrecho de la clase de las penicilinas .
La meticilina fue descubierta en 1960. [1]
Usos médicos
En comparación con otras penicilinas que enfrentan resistencia antimicrobiana debido a la β-lactamasa , es menos activa, se puede administrar solo por vía parenteral y tiene una mayor frecuencia de nefritis intersticial , un efecto adverso de las penicilinas que, por lo demás, es poco común. Sin embargo, la selección de la meticilina dependía del resultado de las pruebas de susceptibilidad de la infección muestreada y, dado que ya no se produce, tampoco se realiza ninguna prueba de rutina para detectarla. También sirvió para determinar en el laboratorio la sensibilidad antibiótica de Staphylococcus aureus a otras penicilinas que enfrentan resistencia a las β-lactamasas; esta función ahora se ha transmitido a otras penicilinas, a saber, la cloxacilina , así como a las pruebas genéticas para detectar la presencia del gen mecA mediante PCR . [ cita requerida ]
Espectro de actividad
En un tiempo, la meticilina se utilizaba para tratar infecciones causadas por ciertas bacterias grampositivas, entre ellas Staphylococcus aureus , Staphylococcus epidermidis , Streptococcus pyogenes y Streptococcus pneumoniae . La meticilina solo es eficaz contra Staphylococcus aureus el 50 % de las veces.
La resistencia a la meticilina se confiere mediante la activación de un nuevo gen de la proteína de unión a la penicilina bacteriana (PBP) mecA , que codifica la proteína PBP2a. La PBP2a funciona de manera similar a otras PBP, pero se une a las β-lactámicas con muy baja afinidad, lo que significa que no compiten de manera eficiente con el sustrato natural de la enzima y no inhiben la biosíntesis de la pared celular. La expresión de PBPA2 confiere resistencia a todas las β-lactámicas. [ cita requerida ]
Estos datos de susceptibilidad se dan para unas cuantas bacterias de importancia médica:
- Staphylococcus aureus : 0,125 – >100 μg/ml
- Staphylococcus aureus resistente a la meticilina (MRSA): 15,6 – >1000 μg/ml
- Streptococcus pneumoniae : 0,39 μg/ml [2]
Mecanismo de acción
Al igual que otros antibióticos betalactámicos, la meticilina actúa inhibiendo la síntesis de las paredes celulares bacterianas . Inhibe la reticulación entre las cadenas de polímeros de peptidoglicano lineal que forman un componente principal de la pared celular de las bacterias grampositivas. Lo hace uniéndose a la enzima transpeptidasa (también conocida como proteínas de unión a la penicilina (PBP)) e inhibiéndola competitivamente. Estas PBP reticulan los glucopéptidos ( D -alanil-alanina ), formando la pared celular de peptidoglicano. La meticilina y otros antibióticos betalactámicos son análogos estructurales de la D -alanil-alanina, y las enzimas transpeptidasas que se unen a ellos a veces se denominan proteínas de unión a la penicilina (PBP). [3]
La meticilina es en realidad un antibiótico betalactámico resistente a la penicilinasa . La penicilinasa es una enzima bacteriana producida por bacterias resistentes a otros antibióticos betalactámicos que hidrolizan el antibiótico, dejándolo inoperativo. La meticilina no se une ni se hidroliza con la penicilinasa, lo que significa que puede matar a las bacterias, incluso si esta enzima está presente.
Química medicinal
La meticilina es resistente a las betalactamasas , que son enzimas secretadas por muchas bacterias resistentes a los antibióticos betalactámicos. La presencia del grupo orto -dimetoxifenilo unido directamente al grupo carbonilo de la cadena lateral del núcleo de la penicilina facilita la resistencia a las betalactamasas, ya que esas enzimas son relativamente intolerantes al impedimento estérico de la cadena lateral . Por lo tanto, es capaz de unirse a las PBP e inhibir la reticulación de los peptidoglicanos , pero no se une a las betalactamasas ni es inactivada por ellas. [ cita requerida ]
Historia
La meticilina fue desarrollada por Beecham en 1959. [4] Anteriormente se utilizaba para tratar infecciones causadas por bacterias grampositivas susceptibles, en particular, organismos productores de penicilinasa como Staphylococcus aureus que de otro modo serían resistentes a la mayoría de las penicilinas.
Su papel en la terapia ha sido reemplazado en gran medida por la oxacilina (usada para pruebas de susceptibilidad antimicrobiana clínica), la flucloxacilina y la dicloxacilina , pero el término Staphylococcus aureus resistente a la meticilina (MRSA) continúa utilizándose para describir las cepas de S. aureus resistentes a todas las penicilinas. [5]
Referencias
- ^ Walker SR (2012). Tendencias y cambios en la investigación y el desarrollo de fármacos. Springer Science & Business Media. pág. 109. ISBN 9789400926592.
- ^ "Datos de susceptibilidad y concentración (CMI) de meticilina sódica" (PDF) . TOKU-E .
- ^ Gladwin M, Trattler B (2004). Microbiología clínica simplificada hasta lo ridículo (3.ª ed.). Miami: MedMaster, Inc.
- ^ Dutfield G (30 de julio de 2009). Derechos de propiedad intelectual e industrias de las ciencias biológicas: pasado, presente y futuro. World Scientific. pp. 140–. ISBN 978-981-283-227-6. Recuperado el 18 de noviembre de 2010 .
- ^ Newsom SW (noviembre de 2004). "MRSA: pasado, presente y futuro". Revista de la Royal Society of Medicine . 97 (11): 509–10. doi :10.1177/014107680409701101. PMC 1079642 . PMID 15520143.
