Vía no mevalonato
La vía no mevalonato —que también aparece como la vía independiente del mevalonato y la vía 2- C -metil- D -eritritol 4-fosfato/1-desoxi- D -xilulosa 5-fosfato ( MEP/DOXP ) —es una vía metabólica alternativa para la biosíntesis de los precursores isoprenoides pirofosfato de isopentenilo (IPP) y pirofosfato de dimetilalilo (DMAPP). [1] [2] [3] El nombre actualmente preferido para esta vía es la vía MEP , ya que MEP es el primer metabolito comprometido en la ruta a IPP .
Biosíntesis de precursores de isoprenoides
La vía del mevalonato (vía MVA o vía de la HMG-CoA reductasa ) y la vía MEP son vías metabólicas para la biosíntesis de precursores de isoprenoides: IPP y DMAPP. Mientras que las plantas utilizan tanto la vía MVA como la MEP, la mayoría de los organismos solo utilizan una de las vías para la biosíntesis de precursores de isoprenoides. En las células vegetales, la biosíntesis de IPP/DMAPP a través de la vía MEP tiene lugar en orgánulos de plástidos , mientras que la biosíntesis a través de la vía MVA tiene lugar en el citoplasma. [4] La mayoría de las bacterias gramnegativas, las cianobacterias fotosintéticas y las algas verdes utilizan solo la vía MEP. [5] Las bacterias que utilizan la vía MEP incluyen patógenos importantes como Mycobacterium tuberculosis . [6]
El IPP y el DMAPP sirven como precursores para la biosíntesis de moléculas isoprenoides (terpenoides) utilizadas en procesos tan diversos como la prenilación de proteínas , el mantenimiento de la membrana celular , la síntesis de hormonas , el anclaje de proteínas y la N -glicosilación en los tres dominios de la vida. [ cita requerida ] En los organismos fotosintéticos, los precursores derivados de MEP se utilizan para la biosíntesis de pigmentos fotosintéticos, como los carotenoides y la cadena fitol de la clorofila y los pigmentos que captan luz. [5]
Se han diseñado bacterias como Escherichia coli para que coexpresen genes de biosíntesis de las vías MEP y MVA . [7] La distribución de los flujos metabólicos entre las vías MEP y MVA se puede estudiar utilizando isotopómeros de 13 C-glucosa . [8]
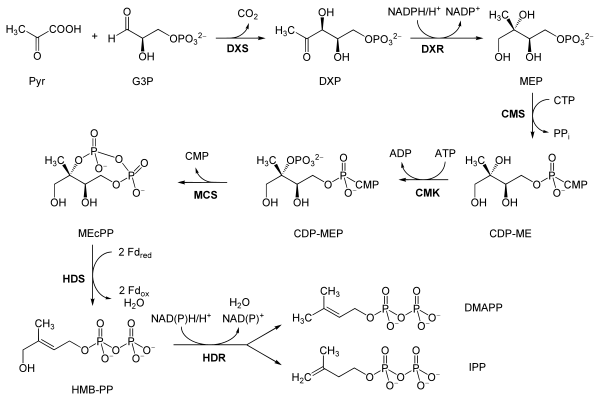
Reacciones
Las reacciones de la vía MEP son las siguientes, tomadas principalmente de Eisenreich y colaboradores, excepto donde las etiquetas en negrita son abreviaturas locales adicionales para ayudar a conectar la tabla con el esquema anterior: [10] [9]
| Reactivos | Enzima | Producto | |
|---|---|---|---|
| Piruvato ( Pyr ) y gliceraldehído 3-fosfato ( G3P ) | Sintetasa DOXP (Dxs; DXP ) | 1-Desoxi-D-xilulosa 5-fosfato (DOXP; DXP ) |  |
| DOXP ( DXP ) | DXP reductoisomerasa (Dxr, IspC; DXR ) | 2-C-metileritritol 4-fosfato (MEP) |  |
| Diputado europeo | 2-C-metil-D-eritritol 4-fosfato citidiltransferasa (YgbP, IspD; CMS ) | 4-difosfocitidil-2-C-metileritritol (CDP-ME) |  |
| CDP-ME | 4-difosfocitidil-2-C-metil-D-eritritol quinasa (YchB, IspE; CMK ) | 4-difosfocitidil-2-C-metil-D-eritritol 2-fosfato (CDP-MEP) |  |
| Diputado europeo del CDP | 2-C-metil-D-eritritol 2,4-ciclodifosfato sintasa ( YgbB , IspF; MCS ) | 2-C-metil-D-eritritol 2,4-ciclodifosfato (MEcPP) |  |
| MEcPP | Sintetasa HMB-PP (GcpE, IspG; HDS ) | Pirofosfato de (E)-4-hidroxi-3-metil-but-2-enilo (HMB-PP) |  |
| HMB-PP | HMB-PP reductasa (LytB, IspH; HDR ) | Pirofosfato de isopentenilo (IPP) y pirofosfato de dimetilalilo (DMAPP) |   |
Investigación sobre inhibición y otras vías
La Dxs, la primera enzima de la vía, es inhibida por retroalimentación por los productos IPP y DMAPP. La Dxs es activa como un homodímero y el mecanismo preciso de inhibición enzimática ha sido debatido en el campo. Se ha propuesto que la IPP/DMAPP compiten con el cofactor TPP. [11] Un estudio más reciente sugirió que la IPP/DMAPP desencadena la monomerización y la posterior degradación de la enzima, a través de la interacción con un sitio de interacción de monómero que difiere del sitio activo de la enzima . [12]
La DXP reductoisomerasa (también conocida como: DXR, DOXP reductoisomerasa, IspC, MEP sintasa) es una enzima clave en la vía MEP. Puede ser inhibida por el producto natural fosmidomicina , que se está estudiando como punto de partida para desarrollar un fármaco candidato antibacteriano o antipalúdico. [13] [14] [15]
El intermediario, HMB-PP , es un activador natural de las células T humanas Vγ9/Vδ2 , la principal población de células T γδ en la sangre periférica, y células que "juegan un papel crucial en la respuesta inmune a los patógenos microbianos". [16]
- Inhibidores de IspH: vía metabólica no mevalonato que es esencial para la mayoría de las bacterias pero que está ausente en los humanos, lo que la convierte en un objetivo ideal para el desarrollo de antibióticos. Esta vía, llamada metil-D-eritritol fosfato (MEP) o vía no mevalonato, es responsable de la biosíntesis de isoprenoides, moléculas necesarias para la supervivencia celular en la mayoría de las bacterias patógenas y, por lo tanto, serán útiles en la mayoría de las bacterias resistentes a los antibacterianos. [17]
Ingeniería metabólica de la vía MEP/No mevalonato
La vía MEP ha sido ampliamente estudiada y diseñada por Escherichia coli , una especie microbiana comúnmente utilizada para investigación y aplicación en laboratorio. [18] IPP y DMAPP, los productos de la vía MEP pueden usarse como sustratos para la producción heteróloga de terpenoides con alto valor para su aplicación en la industria farmacéutica y química. Tras la expresión de genes heterólogos de diferentes organismos, la producción de terpenoides como limoneno , bisaboleno e isopreno podría lograrse en diferentes chasis microbianos. [19] [20] [21] [22] Los estudios que sobreexpresan diferentes genes de biosíntesis de la vía revelaron que la expresión de Dxs e Idi, que catalizan el primer y último paso de la vía MEP, podría aumentar significativamente el rendimiento de los terpenoides derivados de MEP. [19] [22] Dxs como la primera enzima de la vía representa un cuello de botella para el flujo de carbono que entra en la vía. El Idi, que interconvierte IPP en DMAPP y viceversa, parece ser importante para proporcionar el sustrato respectivo que se necesita tras la introducción de un sumidero de carbono heterólogo en cepas modificadas genéticamente. Se ha realizado una gran cantidad de trabajo de ingeniería metabólica sobre la vía MEP en cianobacterias , microbios fotoautotróficos que pueden asimilar el dióxido de carbono de la atmósfera en varios metabolitos que contienen carbono, incluidos los terpenoides. [20] [19] [21] Para la biotecnología, las cianobacterias son, por tanto, una plataforma atractiva para la producción sostenible de compuestos de alto valor.
Referencias
- ^ Rohmer M; Rohmer, Michel (1999). "El descubrimiento de una vía independiente del mevalonato para la biosíntesis de isoprenoides en bacterias, algas y plantas superiores". Nat Prod Rep . 16 (5): 565–574. doi :10.1039/a709175c. PMID 10584331.
- ^ W. Eisenreich; A. Bacher; D. Arigoni; F. Rohdich (2004). "Revisión de la biosíntesis de isoprenoides a través de la vía no mevalonato". Ciencias de la vida celular y molecular . 61 (12): 1401–1426. doi :10.1007/s00018-004-3381-z. PMC 11138651 . PMID 15197467. S2CID 24558920.
- ^ Hunter, WN (2007). "La vía no mevalonato de la biosíntesis de precursores de isoprenoides". Journal of Biological Chemistry . 282 (30): 21573–21577. doi : 10.1074/jbc.R700005200 . PMID 17442674.
- ^ Lichtenthaler H (1999). "La vía de la 1-desoxi-D-xilulosa-5-fosfato de la biosíntesis de isoprenoides en plantas". Revisión anual de fisiología vegetal y biología molecular de plantas . 50 : 47–65. doi :10.1146/annurev.arplant.50.1.47. PMID 15012203.
- ^ ab Vranová, Eva; Coman, Diana; Gruissem, Wilhelm (29 de abril de 2013). "Análisis de red de las vías MVA y MEP para la síntesis de isoprenoides". Revisión anual de biología vegetal . 64 (1): 665–700. doi :10.1146/annurev-arplant-050312-120116. ISSN 1543-5008. PMID 23451776.
- ^ Wiemer, AJ; Hsiao, CH; Wiemer, DF (2010). "Metabolismo de isoprenoides como objetivo terapéutico en patógenos gramnegativos". Temas actuales en química medicinal . 10 (18): 1858–1871. doi :10.2174/156802610793176602. PMID 20615187.
- ^ Martin MJ, Pitera DJ, Withers ST, Newman JD, Keasling JD (2003). "Ingeniería de una vía de mevalonato en Escherichia coli para la producción de terpenoides". Nature Biotechnology . 21 (7): 796–802. doi :10.1038/nbt833. PMID 12778056. S2CID 17214504.
- ^ Orsi E, Beekwilder J, Peek S, Eggink G, Kengen SW, Weusthuis RA (2020). "Análisis de la relación de flujo metabólico mediante marcaje paralelo con 13C de la biosíntesis de isoprenoides en Rhodobacter sphaeroides". Ingeniería Metabólica . 57 : 228–238. doi : 10.1016/j.ymben.2019.12.004 . PMID 31843486.
- ^ ab Qidwai T, Jamal F, Khan MY, Sharma B (2014). "Exploración de dianas farmacológicas en la vía biosintética de isoprenoides para Plasmodium falciparum". Biochemistry Research International . 2014 : 657189. doi : 10.1155/2014/657189 . PMC 4017727. PMID 24864210 . (Retractado, ver doi :10.1155/2022/8426183, PMID 35340427. )
- ^ ab Eisenreich W, Bacher A, Arigoni D, Rohdich F (2004). "Biosíntesis de isoprenoides a través de la vía no mevalonato". Cell. Mol. Life Sci . 61 (12): 1401–26. doi :10.1007/s00018-004-3381-z. PMC 11138651. PMID 15197467. S2CID 24558920 .
- ^ Banerjee, Aparajita; Wu, Yan; Banerjee, Rahul; Li, Yue; Yan, Honggao; Sharkey, Thomas D. (junio de 2013). "La inhibición por retroalimentación de la desoxi-d-xilulosa-5-fosfato sintasa regula la vía del metileritritol 4-fosfato". Journal of Biological Chemistry . 288 (23): 16926–16936. doi : 10.1074/jbc.m113.464636 . ISSN 0021-9258. PMC 3675625 . PMID 23612965.
- ^ Di, Xueni; Ortega-Alarcón, David; Kakumanu, Ramu; Iglesias-Fernández, Javier; Díaz, Lucía; Baidoo, Edward EK; Velázquez-Campoy, Adrián; Rodríguez-Concepción, Manuel; Pérez-Gil, Jordi (8 de mayo de 2023). "Los productos de la vía MEP promueven alostéricamente la monomerización de la desoxi-D-xilulosa-5-fosfato sintasa para regular por retroalimentación su suministro". Comunicaciones de Planta . 4 (3): 100512. doi : 10.1016/j.xplc.2022.100512 . hdl : 10261/335525 . ISSN 2590-3462. PMID 36575800.
- ^ Hale I, O'Neill PM, Berry NG, Odom A, Sharma R (2012). "La vía MEP y el desarrollo de inhibidores como posibles agentes antiinfecciosos". Med. Chem. Commun . 3 (4): 418–433. doi :10.1039/C2MD00298A.
- ^ Jomaa H, Wiesner J, Sanderbrand S, et al. (1999). "Inhibidores de la vía no mevalonato de la biosíntesis de isoprenoides como fármacos antimaláricos". Science . 285 (5433): 1573–6. doi :10.1126/science.285.5433.1573. PMID 10477522.
- ^ C. Zinglé; L. Kuntz; D. Tritsch; C. Grosdemange-Billiard; M. Rohmer (2010). "Biosíntesis de isoprenoides a través de la vía del metileritritol fosfato: variaciones estructurales en torno al ancla y espaciador de fosfonato de la fosmidomicina, un potente inhibidor de la desoxixilulosa fosfato reductoisomerasa". J. Org. Chem. 75 (10): 3203–3207. doi :10.1021/jo9024732. PMID 20429517.
- ^ Eberl M, Hintz M, Reichenberg A, Kollas AK, Wiesner J, Jomaa H (2003). "Biosíntesis de isoprenoides microbianos y activación de células T γδ humanas". FEBS Lett . 544 (1–3): 4–10. doi : 10.1016/S0014-5793(03)00483-6 . PMID 12782281. S2CID 9930822.
- ^ "Un equipo de investigación informa sobre una nueva clase de antibióticos activos contra una amplia gama de bacterias". MDLinx . 23 de diciembre de 2020 . Consultado el 23 de enero de 2023 .[ enlace muerto ]
- ^ Rodríguez-Concepción, Manuel; Boronat, Albert (1 de noviembre de 2002). "Elucidación de la vía del fosfato de metileritritol para la biosíntesis de isoprenoides en bacterias y plástidos. Un hito metabólico logrado mediante genómica". Fisiología vegetal . 130 (3): 1079–1089. doi : 10.1104/pp.007138 . PMC 1540259 . PMID 12427975.
- ^ abc Englund, Elias; Shabestary, Kiyan; Hudson, Elton P.; Lindberg, Pia (1 de septiembre de 2018). "Estudio sistemático de sobreexpresión para encontrar enzimas diana que mejoren la producción de terpenos en Synechocystis PCC 6803, utilizando isopreno como compuesto modelo". Ingeniería metabólica . 49 : 164–177. doi : 10.1016/j.ymben.2018.07.004 . ISSN 1096-7176. PMID 30025762.
- ^ ab Gao, Xiang; Gao, Fang; Liu, Deng; Zhang, Hao; Nie, Xiaoqun; Yang, Chen (13 de abril de 2016). "Ingeniería de la vía del fosfato de metileritritol en cianobacterias para la producción fotosintética de isopreno a partir de CO2". Energy & Environmental Science . 9 (4): 1400–1411. doi :10.1039/C5EE03102H. ISSN 1754-5706.
- ^ ab Rodrigues, João S.; Lindberg, Pia (1 de junio de 2021). "Ingeniería metabólica de Synechocystis sp. PCC 6803 para mejorar la producción de bisaboleno". Metabolic Engineering Communications . 12 : e00159. doi : 10.1016/j.mec.2020.e00159 . ISSN 2214-0301. PMC 7809396 . PMID 33489752.
- ^ ab Du, Fu-Liang; Yu, Hui-Lei; Xu, Jian-He; Li, Chun-Xiu (31 de agosto de 2014). "Producción mejorada de limoneno mediante la optimización de la expresión de los genes de la vía de la biosíntesis de limoneno y MEP en E. coli". Bioresources and Bioprocessing . 1 (1): 10. doi : 10.1186/s40643-014-0010-z . ISSN 2197-4365.