Síntesis de indol de Nenitzescu
| Síntesis de indol de Nenitzescu | |
|---|---|
| Llamado en honor a | Costin Nenițescu |
| Tipo de reacción | Reacción de formación de anillos |
La síntesis de indol de Nenitzescu es una reacción química que forma derivados de indol 5-hidroxi a partir de benzoquinona y ésteres β-aminocrotónicos.

Esta reacción debe su nombre a su descubridor, Costin Nenițescu , quien la informó por primera vez en 1929. [1] Se puede realizar con varias combinaciones diferentes de grupos R, que incluyen sustituyentes metilo, metoxi, etilo, propilo y H. [2] También existe una variación en estado sólido en la que la reacción tiene lugar en un andamio de polímero altamente reticulado. [3] La síntesis es particularmente interesante porque los indoles son la base de varias moléculas bioquímicamente importantes, incluidos los neurotransmisores y una nueva clase de compuestos antitumorales. [4]
Mecanismo
El mecanismo de una reacción de Nenitzescu consiste en una adición de Michael , seguida de un ataque nucleofílico por el enlace pi de la enamina , y luego una eliminación . [5]

La reacción fue publicada por primera vez por Nenitzescu en 1929, [1] y desde entonces ha sido refinada por Allen et al. [2] En su publicación de 1996, Allen y sus colaboradores investigaron los efectos que diferentes sustituyentes en el material de partida de benzoquinona tenían sobre la disposición del producto final. Estos efectos estéricos también dieron evidencia de que uno de los dos mecanismos propuestos actualmente era más probable que el otro, lo que llevó a la publicación del mecanismo que se muestra arriba.
Condiciones
Un estudio preliminar realizado por Katkevica et al. investigó las condiciones de reacción para una síntesis de Nenitzescu e informó sobre el comportamiento de la reacción cuando tiene lugar en varios solventes. [6] Sus resultados indicaron que la reacción funciona mejor en un solvente altamente polar, y se propusieron estudios cinéticos adicionales que involucraban variación del sustrato, reactivos, solventes y la presencia de ácidos y bases de Lewis. Dos años después, Velezheva et al. informaron una versión alternativa de la síntesis utilizando un catalizador de ácido de Lewis . [7] Informan que el efecto catalizador se origina a partir de la activación de la enamina a través de un complejo dicetodienamina-ZnCl 2 .
Sin embargo, a pesar de las mejoras en las condiciones, la síntesis tradicional de Nenitzescu no era adecuada para su uso a escala industrial debido a un rendimiento y una polimerización relativamente bajos en condiciones de reacción normales. Originalmente, se creía que la benzoquinona debía usarse en un exceso del 100% para llevar la reacción hasta su finalización a esta escala, pero Huang et al. informaron que un exceso del 20 al 60% es lo más efectivo. [8] Además, informaron que para las condiciones ideales para una reacción a gran escala, debería haber una relación molar de 1:1,2-1,6 entre la benzoquinona y el 3-aminocrotonato de etilo, y la reacción debería tener lugar alrededor de la temperatura ambiente. Estas condiciones son suficientes para producir lotes de 100 kg o más.
Variaciones y reacciones relacionadas
Una de las variantes más comunes de la reacción de Nenitzescu es la variante en fase sólida . Esta reacción, descrita por primera vez por Ketcha et al. , se muestra a continuación. [3]
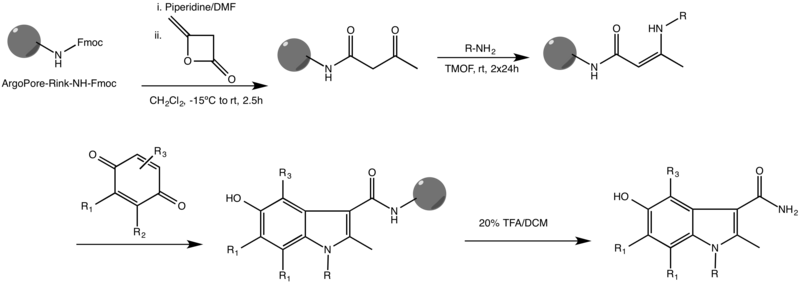
Se lleva a cabo en una resina ArgoPore®-Rink-NH-Fmoc altamente reticulada y funciona con una variedad de sustituyentes en ambos reactivos. También se informaron otras síntesis de indol en fase sólida, algunas de las cuales utilizan diferentes estructuras y catalizadores metálicos para impulsar la reacción hasta su finalización.
También hay una variedad de otras reacciones que dan como resultado el mismo esqueleto de indol. En un artículo de revisión, Taber et al. categorizan estas reacciones en nueve tipos básicos de síntesis de indol: Fischer , Mori, Hemetsberger , Buchwald , Sundberg, Madelung , Nenitzescu, van Leusen y Kanematsu. [9]
Aplicaciones
El esqueleto de 5-hidroxiindol es la base de varias moléculas bioquímicamente importantes. Entre ellas se encuentran la serotonina , un neurotransmisor; la indometacina , un agente antiinflamatorio no esteroide; L-761,066, un inhibidor de la COX-2 ; y LY311727, un inhibidor de la fosfolipasa secretora. [3] Actualmente, una de las aplicaciones más interesantes de la síntesis de Nenitzescu es su capacidad para producir un precursor de compuestos antitumorales. Esta síntesis, informada en 2006, implica la reacción de 1,4,9,10-antradiquinona con varias enaminas. [4] Los productos de esta reacción constituyen una nueva clase de estructuras principales para el diseño de fármacos contra el cáncer.
Referencias
- ^ ab Nenitzescu, CD (1929). "Derivados del 2-metil-5-hidroxiindol". Bull. Soc. Chim. Rumania . 11 : 37–43.
- ^ ab Allen, G.; Pidacks, C.; Weiss, M. (5 de junio de 1996). "Los antibióticos de mitomicina. Estudios sintéticos". J. Am. Chem. Soc. 88 (11): 2536–2544. doi :10.1021/ja00963a032. PMID 5941382.
- ^ abc Ketcha, Daniel M.; Wilson, LJ; Portlock, DE (2000). "La síntesis de indol de Nenitzescu en fase sólida". Tetrahedron Letters . 41 (33): 6253–6257. doi :10.1016/S0040-4039(00)00697-3.
- ^ ab Schenck, Lothar Werner; Kuna, K.; Frank, W.; Albert, A.; Asche, C.; Kucklaender, U. (10 de enero de 2006). "1,4,9,10-Antradiquinona como precursor de compuestos antitumorales". Química bioorgánica y medicinal . 14 (10): 3599–3614. doi :10.1016/j.bmc.2006.01.026. PMID 16458517.
- ^ Li, Jie Jack (2009). Nombre Reacciones, 4ª ed . Berlín: Springer-Verlag. págs. 391–392. ISBN 978-3642010521.
- ^ Katkevica, Daze; Trapencieris, P.; Boman, A.; Kalvins, I.; Lundstedt, T. (2004). "La reacción de Nenitzescu: una selección inicial de condiciones experimentales para mejorar el rendimiento de una reacción modelo". J. Chemometrics . 18 (34): 1883–187. doi :10.1002/cem.863. S2CID 95058789.
- ^ Velezheva, Valeriya S.; Sokolov, AI; Kornienko, AG; Lyssenko, KA; Nelyubina, YV; Godovikov, IA; Peregudov, AS; Mironov, AF (15 de septiembre de 2008). "El papel de un ácido de Lewis en la síntesis del indol de Nenitzescu". Letras de tetraedro . 49 (50): 7106–7109. doi :10.1016/j.tetlet.2008.09.087.
- ^ Huang, Yun-Sheng; Zhang, W.; Zhang, X.; Wang, J. (2010). "Síntesis de fabricación de 5-hidroxi-2-metil-1H-indol". Investigación sobre intermediarios químicos . 36 (8): 975–983. doi :10.1007/s11164-010-0210-x. S2CID 94168531.
- ^ Taber, Douglass F.; Tirunahari, PK (21 de junio de 2011). "Síntesis de indol: una revisión y una clasificación propuesta". Tetrahedron . 67 (38): 7195–7210. doi :10.1016/j.tet.2011.06.040. PMC 4255418 . PMID 25484459.