Prueba de Ames
La prueba de Ames es un método ampliamente utilizado que utiliza bacterias para probar si una sustancia química determinada puede causar mutaciones en el ADN del organismo de prueba. Más formalmente, es un ensayo biológico para evaluar el potencial mutagénico de los compuestos químicos. [1] Una prueba positiva indica que la sustancia química es mutagénica y, por lo tanto, puede actuar como carcinógeno , porque el cáncer a menudo está relacionado con la mutación . La prueba sirve como un ensayo rápido y conveniente para estimar el potencial carcinógeno de un compuesto porque los ensayos carcinógenos estándar en ratones y ratas requieren mucho tiempo (tardan entre dos y tres años en completarse) y son costosos. Sin embargo, se conocen falsos positivos y falsos negativos. [2]
El procedimiento fue descrito en una serie de artículos a principios de la década de 1970 por Bruce Ames y su grupo en la Universidad de California, Berkeley . [3] [4] [5] [6]
Procedimiento general
En el test de Ames se utilizan varias cepas de la bacteria Salmonella typhimurium que presentan mutaciones en genes implicados en la síntesis de histidina . Estas cepas son mutantes auxotróficas , es decir, que necesitan histidina para crecer, pero no pueden producirla. El método prueba la capacidad de la sustancia analizada para crear mutaciones que den como resultado un retorno a un estado "prototrófico", de modo que las células puedan crecer en un medio sin histidina.
Las cepas de prueba están especialmente construidas para detectar mutaciones por desplazamiento del marco de lectura (p. ej., cepas TA-1537 y TA-1538) o puntuales (p. ej., cepa TA-1531) en los genes necesarios para sintetizar histidina, de modo que se puedan identificar mutágenos que actúan a través de diferentes mecanismos. Algunos compuestos son bastante específicos y provocan reversiones en solo una o dos cepas. [4] Las cepas de prueba también presentan mutaciones en los genes responsables de la síntesis de lipopolisacáridos , lo que hace que la pared celular de las bacterias sea más permeable, [5] y en el sistema de reparación por escisión para que la prueba sea más sensible. [6]
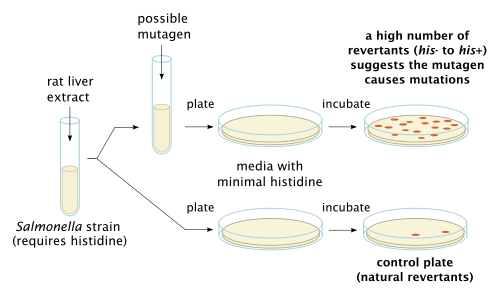
Los organismos más grandes, como los mamíferos, tienen procesos metabólicos que podrían convertir una sustancia química considerada no mutagénica en una que lo sea o una que se considere mutagénica en una que no lo sea. [7] Por lo tanto, para probar de manera más efectiva la mutagenicidad de un compuesto químico en relación con organismos más grandes, se pueden agregar enzimas de hígado de rata en un intento de replicar el efecto de los procesos metabólicos en el compuesto que se está probando en la Prueba de Ames. Opcionalmente, se agrega extracto de hígado de rata para simular el efecto del metabolismo , ya que algunos compuestos, como el benzo[ a ]pireno , no son mutagénicos en sí mismos, pero sus productos metabólicos sí lo son. [3]
Las bacterias se esparcen en una placa de agar con una pequeña cantidad de histidina. Esta pequeña cantidad de histidina en el medio de crecimiento permite que las bacterias crezcan durante un tiempo inicial y tengan la oportunidad de mutar. Cuando la histidina se agota, solo las bacterias que han mutado para obtener la capacidad de producir su propia histidina sobrevivirán. La placa se incuba durante 48 horas. La mutagenicidad de una sustancia es proporcional al número de colonias observadas.
Prueba de Ames y carcinógenos
Los mutágenos identificados mediante la prueba de Ames también son posibles carcinógenos, y los primeros estudios de Ames mostraron que el 90% de los carcinógenos conocidos pueden identificarse mediante esta prueba. [8] Sin embargo, estudios posteriores mostraron la identificación del 50 al 70% de los carcinógenos conocidos. [ cita requerida ] La prueba se utilizó para identificar una serie de compuestos utilizados anteriormente en productos comerciales como carcinógenos potenciales. [9] Los ejemplos incluyen tris (2,3-dibromopropil) fosfato , que se utilizó como retardante de llama en plástico y textiles como ropa de dormir para niños, [10] y furilfuramida , que se utilizó como aditivo antibacteriano en alimentos en Japón en los años 1960 y 1970. De hecho, la furilfuramida había pasado previamente las pruebas con animales, pero pruebas más rigurosas después de su identificación en la prueba de Ames demostraron que era cancerígena. [11] Sus pruebas positivas dieron como resultado que esos productos químicos se retiraran del uso en productos de consumo.
Un resultado interesante de la prueba de Ames es que la curva de respuesta a la dosis utilizando concentraciones variables de la sustancia química es casi siempre lineal, [8] lo que indica que no hay una concentración umbral para la mutagénesis. Por lo tanto, sugiere que, al igual que con la radiación, puede que no haya un umbral seguro para los mutágenos o carcinógenos químicos. [12] [13] Sin embargo, algunos han propuesto que los organismos podrían tolerar niveles bajos de mutágenos debido a mecanismos de protección como la reparación del ADN , y por lo tanto puede existir un umbral para ciertos mutágenos químicos. [14] El propio Bruce Ames argumentó en contra de la extrapolación lineal de la dosis-respuesta de la dosis alta utilizada en pruebas de carcinogénesis en sistemas animales a la dosis más baja de sustancias químicas que normalmente se encuentran en la exposición humana, ya que los resultados pueden ser falsos positivos debido a la respuesta mitogénica causada por la dosis artificialmente alta de sustancias químicas utilizadas en tales pruebas. [15] [16] También advirtió contra la "histeria sobre minúsculas trazas de sustancias químicas que pueden o no causar cáncer", que "elimina por completo los principales riesgos de los que debería estar al tanto". [17]
La prueba de Ames se utiliza a menudo como una de las pruebas iniciales para detectar posibles carcinógenos en medicamentos potenciales, y es una de las ocho pruebas requeridas por la Ley de Pesticidas (EE. UU.) y una de las seis pruebas requeridas por la Ley de Control de Sustancias Tóxicas (EE. UU.). [18]
Limitaciones
Salmonella typhimurium es un procariota, por lo tanto no es un modelo perfecto para humanos. La fracción S9 de hígado de rata se utiliza para imitar las condiciones metabólicas de los mamíferos de modo que se pueda evaluar el potencial mutagénico de los metabolitos formados por una molécula parental en el sistema hepático; sin embargo, existen diferencias en el metabolismo entre humanos y ratas que pueden afectar la mutagenicidad de las sustancias químicas que se están probando. [19] Por lo tanto, la prueba se puede mejorar mediante el uso de la fracción S9 de hígado humano; su uso estaba limitado anteriormente por su disponibilidad, pero ahora está disponible comercialmente y, por lo tanto, puede ser más factible. [20] Se ha creado un modelo in vitro adaptado para células eucariotas, por ejemplo, levadura.
Los mutágenos identificados en la prueba de Ames no necesariamente tienen que ser cancerígenos, y se requieren más pruebas para cualquier carcinógeno potencial identificado en la prueba. Los medicamentos que contienen la fracción de nitrato a veces dan positivo en la prueba de Ames cuando en realidad son seguros. Los compuestos de nitrato pueden generar óxido nítrico , una molécula de señal importante que puede dar un falso positivo. La nitroglicerina es un ejemplo que da un Ames positivo pero que todavía se utiliza en el tratamiento hoy en día. Sin embargo, los nitratos en los alimentos pueden reducirse por la acción bacteriana a nitritos que se sabe que generan carcinógenos al reaccionar con aminas y amidas. Se necesitan estudios toxicológicos y de resultados prolongados con estos compuestos para refutar un resultado positivo en la prueba de Ames.
Método de fluctuación


La prueba de Ames se desarrolló inicialmente utilizando placas de agar (técnica de incorporación de placa), como se describió anteriormente. Desde entonces, se ha desarrollado una alternativa a la realización de la prueba de Ames, que se conoce como el "método de fluctuación". Esta técnica es la misma en concepto que el método basado en agar, con bacterias que se agregan a una mezcla de reacción con una pequeña cantidad de histidina , lo que permite que las bacterias crezcan y muten, volviendo a sintetizar su propia histidina. Al incluir un indicador de pH, la frecuencia de mutación se cuenta en microplacas como el número de pocillos que han cambiado de color (causado por una caída del pH debido a los procesos metabólicos de reproducción de las bacterias). Al igual que con la prueba de Ames tradicional, la muestra se compara con la tasa de fondo natural de mutación inversa para establecer la genotoxicidad de una sustancia. El método de fluctuación se realiza completamente en cultivo líquido y se puntúa contando el número de pocillos que se vuelven amarillos de morados en microplacas de 96 o 384 pocillos.
En el método de placa de 96 pocillos, la frecuencia de mutación se cuenta como el número de pocillos de 96 que han cambiado de color. Las placas se incuban durante un máximo de cinco días, contando las colonias mutadas (amarillas) cada día y comparándolas con la tasa de fondo de mutación inversa utilizando tablas de significancia establecidas para determinar las diferencias significativas entre la tasa de fondo de mutación y la de las muestras analizadas.
En el método de microfluctuación en placa de 384 pocillos, más reducido, la frecuencia de mutación se contabiliza como el número de pocillos de 48 que han cambiado de color después de 2 días de incubación. Se analiza una muestra de prueba en 6 niveles de dosis con dosis cero (de fondo) y controles positivos simultáneos que caben todos en una placa de 384 pocillos. El ensayo se realiza por triplicado para proporcionar solidez estadística. Utiliza las cepas de prueba recomendadas por la Guía 471 de la OCDE (auxótrofos de histidina y auxótrofos de triptófano).
El método de fluctuación es comparable al método tradicional de vertido en placa en términos de sensibilidad y precisión, sin embargo, tiene una serie de ventajas: necesita menos muestra de prueba, tiene un punto final colorimétrico simple, contar el número de pocillos positivos de un posible 96 o 48 pocillos requiere mucho menos tiempo que contar colonias individuales en una placa de agar. Hay varios kits comerciales disponibles. La mayoría de los kits tienen componentes consumibles en un estado listo para usar, incluidas bacterias liofilizadas, y las pruebas se pueden realizar utilizando pipetas multicanal. El método de fluctuación también permite probar volúmenes más altos de muestras acuosas (hasta 75% v/v), lo que aumenta la sensibilidad y extiende su aplicación a mutágenos ambientales de bajo nivel. [21]
Referencias
- ^ Mortelmans K, Zeiger E (noviembre de 2000). "El ensayo de mutagenicidad de Ames Salmonella/microsoma". Mutation Research . 455 (1–2): 29–60. Bibcode :2000MRFMM.455...29M. doi :10.1016/S0027-5107(00)00064-6. PMID 11113466.
- ^ Charnley G (2002). "Prueba de Ames". Enciclopedia de Salud Pública . eNotes.com. Archivado desde el original el 4 de febrero de 2009 . Consultado el 2 de mayo de 2014 .
- ^ ab Ames BN, Durston WE, Yamasaki E, Lee FD (agosto de 1973). "Los carcinógenos son mutágenos: un sistema de prueba simple que combina homogeneizados de hígado para la activación y bacterias para la detección". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 70 (8): 2281–5. Bibcode :1973PNAS...70.2281A. doi : 10.1073/pnas.70.8.2281 . PMC 433718 . PMID 4151811.
- ^ ab Ames BN, Gurney EG, Miller JA, Bartsch H (noviembre de 1972). "Carcinógenos como mutágenos de cambio de marco: metabolitos y derivados de 2-acetilaminofluoreno y otros carcinógenos de aminas aromáticas". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 69 (11): 3128–32. Bibcode :1972PNAS...69.3128A. doi : 10.1073/pnas.69.11.3128 . PMC 389719 . PMID 4564203.
- ^ ab Ames BN, Lee FD, Durston WE (marzo de 1973). "Un sistema de prueba bacteriana mejorado para la detección y clasificación de mutágenos y carcinógenos". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 70 (3): 782–6. Bibcode :1973PNAS...70..782A. doi : 10.1073/pnas.70.3.782 . PMC 433358 . PMID 4577135.
- ^ ab McCann J, Spingarn NE, Kobori J, Ames BN (marzo de 1975). "Detección de carcinógenos como mutágenos: cepas bacterianas de prueba con plásmidos de factor R". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 72 (3): 979–83. Bibcode :1975PNAS...72..979M. doi : 10.1073/pnas.72.3.979 . PMC 432447 . PMID 165497.
- ^ Hartwell L, Goldberg M, Hood L, Reynolds A, Silver L (2011). Genética: de los genes a los genomas (4.ª ed.). Nueva York: McGraw-Hill. ISBN 978-0-07-352526-6.OCLC 317623365 .
- ^ ab McCann J, Choi E, Yamasaki E, Ames BN (diciembre de 1975). "Detección de carcinógenos como mutágenos en la prueba Salmonella/microsoma: ensayo de 300 sustancias químicas". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 72 (12): 5135–9. Bibcode :1975PNAS...72.5135M. doi : 10.1073/pnas.72.12.5135 . PMC 388891 . PMID 1061098.
- ^ Ames BN (mayo de 1979). "Identificación de sustancias químicas ambientales que causan mutaciones y cáncer" (PDF) . Science . 204 (4393): 587–93. Bibcode :1979Sci...204..587A. doi :10.1126/science.373122. JSTOR 1748159. PMID 373122.
- ^ Prival MJ, McCoy EC, Gutter B, Rosendranz HS (enero de 1977). "Tris(2,3-dibromopropil) fosfato: mutagenicidad de un retardante de llama ampliamente utilizado". Science . 195 (4273): 76–8. Bibcode :1977Sci...195...76P. doi :10.1126/science.318761. PMID 318761.
- ^ Hayatsu, Hiroka (1991), Mutágenos en los alimentos: detección y prevención, CRC Press , pp. 286 páginas, ISBN 978-0-8493-5877-7
- ^ Teasdale A (2011). Impurezas genotóxicas: estrategias para su identificación y control . Wiley-Blackwell. ISBN 978-0-470-49919-1.
- ^ Tubiana M (septiembre de 1992). "El efecto carcinógeno de la exposición a dosis bajas de carcinógenos". British Journal of Industrial Medicine . 49 (9): 601–5. doi :10.1136/oem.49.9.601. PMC 1039303 . PMID 1390264.
- ^ Jenkins GJ, Doak SH, Johnson GE, Quick E, Waters EM, Parry JM (noviembre de 2005). "¿Existen umbrales de respuesta a la dosis para los agentes alquilantes genotóxicos?". Mutagénesis . 20 (6): 389–98. doi : 10.1093/mutage/gei054 . PMID 16135536.
- ^ Forman D (agosto de 1991). "Ames, la prueba de Ames y las causas del cáncer". BMJ . 303 (6800): 428–9. doi :10.1136/bmj.303.6800.428. PMC 1670593 . PMID 1912830.
- ^ Ames BN, Gold LS (octubre de 1990). "Carcinogénesis química: demasiados carcinógenos en roedores". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 87 (19): 7772–6. Bibcode :1990PNAS...87.7772A. doi : 10.1073/pnas.87.19.7772 . PMC 54830 . PMID 2217209.
- ^ Twombly R (septiembre de 2001). "Informe federal sobre carcinógenos estrena nueva lista de nominados". Journal of the National Cancer Institute . 93 (18): 1372. doi : 10.1093/jnci/93.18.1372 . PMID 11562386.
- ^ Farmer PB, Walker JM (2006). La base molecular del cáncer. Krieger Publishing Company. ISBN 978-0-7099-1044-2.
- ^ Hakura A, Suzuki S, Satoh T (enero de 1999). "Ventajas del uso de S9 de hígado humano en la prueba de Ames". Mutation Research . 438 (1): 29–36. Bibcode :1999MRGTE.438...29H. doi :10.1016/s1383-5718(98)00159-4. PMID 9858674.
- ^ Hakura A, Suzuki S, Satoh T (2004). "Mejora de la prueba de Ames utilizando la preparación de hígado humano S9". En Yan Z, Caldwell G (eds.). Optimización en el descubrimiento de fármacos: métodos in vitro . Métodos en farmacología y toxicología. Humana Press. ISBN 978-1-58829-332-9.
- ^ Bridges BA (noviembre de 1980). "La prueba de fluctuación". Archivos de toxicología . 46 (1–2): 41–4. Bibcode :1980ArTox..46...41B. doi :10.1007/BF00361244. PMID 7235997. S2CID 23769437.
Lectura adicional
- Phillipson, Caroline E.; Ioannides, Costas (1989-03-01). "Acción metabólica de los hidrocarburos aromáticos policíclicos sobre mutágenos en la prueba de Ames por varias especies animales, incluido el hombre". Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis . 211 (1): 147–151. Bibcode :1989MRFMM.211..147P. doi :10.1016/0027-5107(89)90115-2. ISSN 0027-5107. PMID 2493576.
- McKinnell RG (6 de noviembre de 2015). La comprensión, la prevención y el control del cáncer humano: la obra histórica y las vidas de Elizabeth Cavert Miller y James A. Miller. BRILL. ISBN 9789004286801.
- Claxton LD, Umbuzeiro GD, DeMarini DM (noviembre de 2010). "El ensayo de mutagenicidad de Salmonella: el estetoscopio de la toxicología genética para el siglo XXI". Environmental Health Perspectives . 118 (11): 1515–22. Bibcode :2010EnvHP.118.1515C. doi :10.1289/ehp.1002336. PMC 2974687 . PMID 20682480.