Nanotubo de efecto túnel
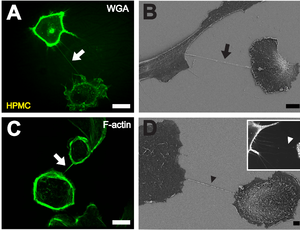
B Representación de un TNT (flecha negra) entre dos células con microscopía electrónica de barrido. Barra de escala: 10 μm.
C F-actina marcada con fluorescencia (flecha blanca) presente en los TNT entre HPMC individuales. Barra de escala: 20 μm.
D Imagen de microscopio electrónico de barrido de un precursor potencial de TNT (punta de flecha negra). El inserto muestra una imagen microscópica de fluorescencia de protuberancias similares a filopodios (punta de flecha blanca) que se acercan a una célula vecina. Barra de escala: 2 μm. [1]
Un nanotubo de efecto túnel (TNT) o nanotubo de membrana es un término que se ha aplicado a las protuberancias del citoesqueleto que se extienden desde la membrana plasmática y que permiten que diferentes células animales se conecten a grandes distancias, a veces más de 100 μm entre ciertos tipos de células. [2] [3] [4] Los nanotubos de efecto túnel que tienen menos de 0,7 micrómetros de diámetro, tienen una estructura de actina y transportan porciones de membrana plasmática entre células en ambas direcciones. Los TNT más grandes (>0,7 μm) contienen una estructura de actina con microtúbulos y/o filamentos intermedios , y pueden transportar componentes como vesículas y orgánulos entre células, incluidas mitocondrias completas . [5] [6] [7] El diámetro de los TNT varía de 0,05 μm a 1,5 μm y pueden alcanzar longitudes de varios diámetros celulares. [7] [8] Se han observado dos tipos de TNT: de extremo abierto y de extremo cerrado. Los TNT de extremo abierto conectan el citoplasma de dos células. Los TNT de extremo cerrado no tienen citoplasma continuo ya que hay una capa de unión en hendidura que solo permite que pequeñas moléculas e iones fluyan entre las células. [9] Estas estructuras han demostrado estar involucradas en la comunicación de célula a célula, la transferencia de ácidos nucleicos como ARNm y miARN entre células en cultivo o en un tejido , y la propagación de patógenos o toxinas como el VIH y los priones . [10] [11] [12] [13 ] [14] [3] Se ha observado que los TNT tienen una vida útil que va desde unos pocos minutos hasta varias horas, y varias proteínas han sido implicadas en su formación e inhibición, incluidas muchas que interactúan con Arp2/3. [15] [16]
Historia

Los nanotubos de membrana se describieron por primera vez en un artículo de Cell de 1999 que examinaba el desarrollo de los discos imaginales de las alas de Drosophila melanogaster . [17] Más recientemente, un artículo de Science publicado en 2004 describió estructuras que conectaban células PC12 entre sí, así como otros tipos de cultivos celulares. [7] [18] Este estudio acuñó el término "nanotubos de tunelización" y también mostró que la formación de nanotubos entre células está correlacionada con la transferencia de membrana y orgánulos. [7] Desde estas publicaciones, se han registrado más estructuras similares a TNT, que contienen niveles variables de F-actina, microtúbulos y otros componentes, pero que permanecen relativamente homogéneas en términos de composición. [15]
Formación
En la formación de nanotubos pueden intervenir diversos mecanismos, entre ellos, controles moleculares e interacciones entre células.
Se han propuesto dos mecanismos principales para la formación de TNT. El primero implica protuberancias citoplasmáticas que se extienden de una célula a otra, donde se fusionan con la membrana de la célula diana. [7] El otro mecanismo ocurre cuando dos células previamente conectadas se alejan una de la otra y los TNT permanecen como puentes entre las dos células. [3] [19]
Inducción
Se ha demostrado que algunas células dendríticas y monocitos THP-1 se conectan a través de nanotubos de efecto túnel y muestran evidencia de flujo de calcio cuando se exponen a estímulos bacterianos o mecánicos. Se ha demostrado que la señalización mediada por TNT produce propagación en las células diana, similar a los lamelipodios que se producen cuando las células dendríticas se exponen a productos bacterianos. Los TNT demostrados en este estudio se propagaron a una velocidad inicial de 35 micrómetros/segundo y se ha demostrado que conectan monocitos THP-1 con nanotubos de hasta 100 micrómetros de longitud. [20]
La exposición a la fosfatidilserina ha demostrado la capacidad de guiar la formación de TNT desde células madre mesenquimales (MSC) a una población de células lesionadas. [21] Se ha demostrado que la proteína S100A4 y su receptor guían la dirección del crecimiento de TNT, ya que p53 activa la caspasa 3 para escindir S100A4 en la célula iniciadora, generando así un gradiente en el que la célula objetivo tiene mayores cantidades de la proteína. [22] Estos hallazgos sugieren que los gradientes quimiotácticos pueden estar involucrados en la inducción de TNT.
Un estudio encontró que el contacto entre células era necesario para la formación de puentes de nanotubos entre células T. [3] La activación de p53 también se ha implicado como un mecanismo necesario para el desarrollo de TNT , ya que se encontró que los genes descendentes regulados positivamente por p53 (a saber, EGFR , Akt , PI3K y mTOR ) estaban involucrados en la formación de nanotubos después del tratamiento con peróxido de hidrógeno y la inanición de suero. [23] Se ha demostrado que la conexina-43 promueve la conexión entre las células del estroma de la médula ósea (BMSC) y las células epiteliales alveolares , lo que conduce a la formación de nanotubos. [24]
También se ha demostrado que el estrés celular por rotenona o TNF-α induce la formación de TNT entre las células epiteliales. [25] Se ha demostrado que la inflamación por lipopolisacáridos o interferón-γ aumenta la expresión de proteínas relacionadas con la formación de TNT. [26]
Inhibición
Si bien los TNT tienen muchos componentes, sus principales inhibidores funcionan bloqueando o limitando la formación de actina. Las estructuras similares a TNT llamadas streamers, que son protuberancias extremadamente delgadas, no se formaron cuando se cultivaron con citocalasina D , un compuesto despolimerizador de F-actina . [27] [28] Un estudio separado que utilizó citocalasina B descubrió que impactó en la formación de TNT sin la destrucción de los TNT existentes. [29] Se descubrió que la latrunculina-B , otro compuesto despolimerizador de F-actina, bloqueaba completamente la formación de TNT. [7] El bloqueo de CD38 , que había sido implicado en la liberación de mitocondrias por los astrocitos , también disminuyó significativamente la formación de TNT. [30] [31]
Se sabe que TNFAIP2 , también llamado M-Sec, media la formación de TNT, y la eliminación de esta proteína por shRNA redujo el desarrollo de TNT en las células epiteliales en aproximadamente dos tercios. [26]
La inhibición directa de Arp2/3 tuvo diferentes efectos según el tipo de célula. En las células oculares y los macrófagos humanos, el bloqueo de Arp2/3 provocó una disminución de la formación de TNT. Sin embargo, dicha inhibición en las células neuronales provocó un aumento de la cantidad de células conectadas a través de TNT, al tiempo que disminuyó la cantidad total de TNT que conectaban las células. [32]
Papel en la transferencia intercelular
Mitocondrias
Los nanotubos de efecto túnel se han implicado como un mecanismo por el cual mitocondrias enteras pueden ser transferidas de célula a célula. [7] Un estudio reciente en Nature Nanotechnology ha informado que las células cancerosas pueden secuestrar las mitocondrias de las células inmunes a través de nanotubos de efecto túnel físicos. [34] El daño al ADN mitocondrial parece ser el desencadenante principal para la formación de TNTs para traficar mitocondrias enteras, aunque el umbral exacto de daño necesario para inducir la formación de TNTs aún se desconoce. [35] Se encontró que la velocidad máxima de las mitocondrias que viajan sobre TNTs era de aproximadamente 80 nm /s, menor que la velocidad medida de 100-1400 nm/s de transporte axonal de mitocondrias; esto podría deberse al diámetro más pequeño de los TNTs que inhibe la migración mitocondrial. [36]
En un estudio, Ahmad et al . utilizaron cuatro líneas de células madre mesenquimales, cada una expresando un fenotipo diferente de la Rho-GTPasa Miro1; un nivel más alto de Miro1 se asoció con una transferencia mitocondrial más eficiente a través de TNT. [25] Varios estudios han demostrado, a través del bloqueo selectivo de la formación de TNT, que los TNT son un mecanismo primario para el tráfico de mitocondrias completas entre células heterogéneas. [37] [38] [39]
Un uso de este fenómeno es en la recuperación de ataques cardíacos . [40] Cuando las células del músculo cardíaco se lesionan por falta de oxígeno, las mitocondrias dañadas liberan especies reactivas de oxígeno, que hacen que las células madre mesenquimales cercanas produzcan y donen mitocondrias sanas a las células musculares dañadas a través de TNT. [40]
Potencial de acción
Se ha demostrado que los nanotubos tunelizadores propagan potenciales de acción a través de sus extensiones del retículo endoplásmico que propagan la entrada de Ca 2+ mediante difusión activa. [41]
Virus
Muchos virus pueden transferir sus proteínas a células conectadas a TNT. Incluso se ha descubierto que ciertos tipos, como el de la gripe, transfieren su genoma a través de TNT. [42] Se ha descubierto que más de dos docenas de tipos de virus transfieren a través de TNT y/o modulan el virus. [43] Un estudio de 2022 sugiere que el SARS-CoV-2 construye nanotubos de tunelización a partir de las células de la nariz para acceder al cerebro . [44] [45]
El VIH también parece propagarse a través de TNT, específicamente entre células dendríticas . [40] Los investigadores han descubierto que los "no progresadores a largo plazo" del VIH, que pueden controlar el virus sin terapia antirretroviral, tienen un defecto en la capacidad de sus células dendríticas para crear TNT. [40]
Priones
Los priones también pueden propagarse a través de TNT. [40]
Nanomedicina
Los nanotubos de efecto túnel tienen el potencial de ser utilizados en aplicaciones de nanomedicina, ya que han demostrado la capacidad de transferir dichos tratamientos entre células. Las aplicaciones futuras buscan inhibir los TNT para evitar que la toxicidad de la nanomedicina llegue a las células vecinas, o promover la formación de TNT para aumentar los efectos positivos del medicamento. [46]
Estructuras similares al TNT
Si bien las estructuras similares a TNT están formadas por protuberancias celulares del citoesqueleto, su diferencia fundamental con los TNT radica en la conexión entre dos células. Las estructuras similares a TNT no comparten contenidos intracelulares, como iones o moléculas pequeñas, entre células conectadas, una característica que está presente tanto en los TNT de extremo abierto como en los de extremo cerrado. [9]
Una estructura similar a la TNT llamada citonema permite los intercambios entre centros de señalización. Se ha observado la formación de citonemas hacia un gradiente homólogo de FGF , lo que sugiere que los controles quimiotácticos también pueden inducir la formación de estructuras similares a la TNT. [17] Sin embargo, los citonemas no siempre conectan la membrana entre dos células y pueden actuar únicamente como sensores ambientales. [28]
Los plasmodesmos se han identificado como canales funcionales que interconectan las células vegetales, y los estrómulos interconectan los plástidos . [47] [48]
Los miopodios son extensiones citoplasmáticas ricas en actina que se han observado en Drosophila embrionaria . Se han observado estructuras similares en Xenopus y modelos de ratón . [15] Se han observado protuberancias celulares que contienen actina denominadas "streamers" en células B cultivadas . [28]
Se ha modelado el transporte vesicular en nanotubos de membrana utilizando un enfoque continuo. [49] Se han investigado diversos nanotubos sintéticos, basados en el apilamiento de péptidos cíclicos y otras moléculas cíclicas. [50]
Véase también
Referencias
- ^ Ranzinger J, Rustom A, Abel M, Leyh J, Kihm L, Witkowski M, et al. (27 de diciembre de 2011). Bereswill S (ed.). "La acción de los nanotubos entre las células mesoteliales humanas revela nuevos aspectos de las respuestas inflamatorias". PLOS ONE . 6 (12): e29537. Bibcode :2011PLoSO...629537R. doi : 10.1371/journal.pone.0029537 . PMC 3246504 . PMID 22216308.
- ^ Abounit S, Zurzolo C (marzo de 2012). "Conexión a través de nanotubos de efecto túnel: desde señales eléctricas hasta transferencia de orgánulos". Journal of Cell Science . 125 (Pt 5): 1089–1098. doi : 10.1242/jcs.083279 . PMID 22399801. S2CID 8433589.
- ^ abcd Sowinski S, Jolly C, Berninghausen O, Purbhoo MA, Chauveau A, Köhler K, et al. (febrero de 2008). "Los nanotubos de membrana conectan físicamente las células T a largas distancias, lo que presenta una nueva ruta para la transmisión del VIH-1". Nature Cell Biology . 10 (2): 211–219. doi :10.1038/ncb1682. PMID 18193035. S2CID 25410308.
- ^ Davis DM, Sowinski S (junio de 2008). "Nanotubos de membrana: conexiones dinámicas a larga distancia entre células animales". Nature Reviews. Molecular Cell Biology . 9 (6): 431–436. doi :10.1038/nrm2399. PMID 18431401. S2CID 8136865.
- ^ Resnik N, Erman A, Veranič P, Kreft ME (octubre de 2019). "Triple etiquetado de filamentos de actina, filamentos intermedios y microtúbulos para una amplia aplicación en biología celular: descubrimiento de la composición del citoesqueleto en nanotubos de efecto túnel". Histoquímica y biología celular . 152 (4): 311–317. doi :10.1007/s00418-019-01806-3. PMID 31392410. S2CID 199491883.
- ^ Onfelt B, Nedvetzki S, Benninger RK, Purbhoo MA, Sowinski S, Hume AN, et al. (diciembre de 2006). "Los nanotubos de membrana estructuralmente distintos entre los macrófagos humanos favorecen el tráfico vesicular a larga distancia o la navegación de las bacterias". Journal of Immunology . 177 (12): 8476–8483. doi : 10.4049/jimmunol.177.12.8476 . PMID 17142745.
- ^ abcdefgh Rustom A, Saffrich R, Markovic I, Walther P, Gerdes HH (febrero de 2004). "Autopistas nanotubulares para el transporte de orgánulos intercelulares". Science . 303 (5660): 1007–1010. Bibcode :2004Sci...303.1007R. doi :10.1126/science.1093133. PMID 14963329. S2CID 37863055.
- ^ Wang ZG, Liu SL, Tian ZQ, Zhang ZL, Tang HW, Pang DW (noviembre de 2012). "Transporte intercelular impulsado por miosina de aglutinina de germen de trigo mediado por nanotubos de membrana entre células de cáncer de pulmón humano". ACS Nano . 6 (11): 10033–10041. doi :10.1021/nn303729r. PMID 23102457.
- ^ ab Zurzolo C (agosto de 2021). "Nanotubos tunelizados: remodelando la conectividad". Current Opinion in Cell Biology . Tráfico de membranas. 71 : 139–147. doi : 10.1016/j.ceb.2021.03.003 . PMID 33866130. S2CID 233298036.
- ^ Onfelt B, Davis DM (noviembre de 2004). "¿Pueden los nanotubos de membrana facilitar la comunicación entre células inmunes?". Biochemical Society Transactions . 32 (Pt 5): 676–678. doi :10.1042/BST0320676. PMID 15493985. S2CID 32181738.
- ^ Haimovich G, Dasgupta S, Gerst JE (febrero de 2021). "Transferencia de ARN a través de nanotubos de tunelización". Biochemical Society Transactions . 49 (1): 145–160. doi :10.1042/BST20200113. PMID 33367488. S2CID 229689880.
- ^ Haimovich G, Ecker CM, Dunagin MC, Eggan E, Raj A, Gerst JE, Singer RH (noviembre de 2017). "Tráfico intercelular de ARNm a través de extensiones similares a nanotubos de membrana en células de mamíferos". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 114 (46): E9873–E9882. Bibcode :2017PNAS..114E9873H. doi : 10.1073/pnas.1706365114 . PMC 5699038 . PMID 29078295.
- ^ Belting M, Wittrup A (diciembre de 2008). "Los nanotubos, los exosomas y los péptidos que se unen a los ácidos nucleicos proporcionan nuevos mecanismos de comunicación intercelular en células eucariotas: implicaciones para la salud y la enfermedad". The Journal of Cell Biology . 183 (7): 1187–1191. doi :10.1083/jcb.200810038. PMC 2606965 . PMID 19103810.
- ^ Gousset K, Schiff E, Langevin C, Marijanovic Z, Caputo A, Browman DT, et al. (marzo de 2009). "Los priones secuestran nanotubos tunelizadores para su propagación intercelular". Nature Cell Biology . 11 (3): 328–336. doi :10.1038/ncb1841. PMID 19198598. S2CID 30793469.
- ^ abc Gurke S, Barroso JF, Gerdes HH (mayo de 2008). "El arte de la comunicación celular: los nanotubos tunelizados cierran la brecha". Histoquímica y biología celular . 129 (5): 539–550. doi :10.1007/s00418-008-0412-0. PMC 2323029 . PMID 18386044.
- ^ Hanna SJ, McCoy-Simandle K, Miskolci V, Guo P, Cammer M, Hodgson L, Cox D (agosto de 2017). "El papel de las Rho-GTPasas y la polimerización de actina durante la biogénesis de nanotubos de efecto túnel de macrófagos". Scientific Reports . 7 (1): 8547. Bibcode :2017NatSR...7.8547H. doi :10.1038/s41598-017-08950-7. PMC 5561213 . PMID 28819224.
- ^ ab Ramírez-Weber FA, Kornberg TB (mayo de 1999). "Citonemas: procesos celulares que se proyectan al centro principal de señalización en discos imaginales de Drosophila". Cell . 97 (5): 599–607. doi : 10.1016/S0092-8674(00)80771-0 . PMID 10367889. S2CID 15789546.
- ^ Onfelt B, Nedvetzki S, Yanagi K, Davis DM (agosto de 2004). "Vanguardia: los nanotubos de membrana conectan las células inmunes". Journal of Immunology . 173 (3): 1511–1513. doi : 10.4049/jimmunol.173.3.1511 . PMID 15265877.
- ^ Sherer NM, Lehmann MJ, Jimenez-Soto LF, Horensavitz C, Pypaert M, Mothes W (marzo de 2007). "Los retrovirus pueden establecer puentes filopodiales para una transmisión eficiente de célula a célula". Nature Cell Biology . 9 (3): 310–315. doi :10.1038/ncb1544. PMC 2628976 . PMID 17293854.
- ^ Watkins SC, Salter RD (septiembre de 2005). "Conectividad funcional entre células inmunes mediada por nanotúbulos tunelizadores". Inmunidad . 23 (3): 309–318. doi : 10.1016/j.immuni.2005.08.009 . PMID 16169503.
- ^ Liu K, Ji K, Guo L, Wu W, Lu H, Shan P, Yan C (marzo de 2014). "Las células madre mesenquimales rescatan células endoteliales lesionadas en un modelo de isquemia-reperfusión in vitro mediante transferencia mitocondrial mediada por una estructura similar a la de un nanotubo tunelizador". Microvascular Research . 92 : 10–18. doi :10.1016/j.mvr.2014.01.008. PMID 24486322.
- ^ Sun X, Wang Y, Zhang J, Tu J, Wang XJ, Su XD, et al. (diciembre de 2012). "Determinación de la dirección de nanotubos de efecto túnel en neuronas y astrocitos". Muerte celular y enfermedad . 3 (12): e438. doi :10.1038/cddis.2012.177. PMC 3542613 . PMID 23222508.
- ^ Wang Y, Cui J, Sun X, Zhang Y (abril de 2011). "El desarrollo de nanotubos de efecto túnel en astrocitos depende de la activación de p53". Muerte celular y diferenciación . 18 (4): 732–742. doi :10.1038/cdd.2010.147. PMC 3131904 . PMID 21113142.
- ^ Islam MN, Das SR, Emin MT, Wei M, Sun L, Westphalen K, et al. (abril de 2012). "La transferencia mitocondrial desde células estromales derivadas de la médula ósea a los alvéolos pulmonares protege contra la lesión pulmonar aguda". Nature Medicine . 18 (5): 759–765. doi :10.1038/nm.2736. PMC 3727429 . PMID 22504485.
- ^ ab Ahmad T, Mukherjee S, Pattnaik B, Kumar M, Singh S, Kumar M, et al. (mayo de 2014). "Miro1 regula el transporte mitocondrial intercelular y mejora la eficacia del rescate de células madre mesenquimales". The EMBO Journal . 33 (9): 994–1010. doi :10.1002/embj.201386030. PMC 4193933 . PMID 24431222.
- ^ ab Hase K, Kimura S, Takatsu H, Ohmae M, Kawano S, Kitamura H, et al. (diciembre de 2009). "M-Sec promueve la formación de nanotubos de membrana al interactuar con Ral y el complejo de exocisto". Nature Cell Biology . 11 (12): 1427–1432. doi :10.1038/ncb1990. PMID 19935652. S2CID 1388030.
- ^ Austefjord MW, Gerdes HH, Wang X (enero de 2014). "Nanotubos de efecto túnel: diversidad en morfología y estructura". Biología comunicativa e integradora . 7 (1): e27934. doi :10.4161/cib.27934. PMC 3995728 . PMID 24778759.
- ^ abc Austefjord MW, Gerdes HH, Wang X (enero de 2014). "Nanotubos de efecto túnel: diversidad en morfología y estructura". Biología comunicativa e integradora . 7 (1): e27934. doi :10.4161/cib.27934. PMC 3995728 . PMID 24778759.
- ^ Bukoreshtliev NV, Wang X, Hodneland E, Gurke S, Barroso JF, Gerdes HH (mayo de 2009). "El bloqueo selectivo de la formación de nanotubos de efecto túnel (TNT) inhibe la transferencia de orgánulos intercelulares entre células PC12". FEBS Letters . 583 (9): 1481–1488. doi :10.1016/j.febslet.2009.03.065. PMID 19345217. S2CID 13528434.
- ^ Hayakawa K, Esposito E, Wang X, Terasaki Y, Liu Y, Xing C, et al. (julio de 2016). "Transferencia de mitocondrias desde astrocitos a neuronas después de un accidente cerebrovascular". Nature . 535 (7613): 551–555. Bibcode :2016Natur.535..551H. doi :10.1038/nature18928. PMC 4968589 . PMID 27466127.
- ^ Marlein CR, Piddock RE, Mistry JJ, Zaitseva L, Hellmich C, Horton RH, et al. (mayo de 2019). "El tráfico mitocondrial impulsado por CD38 promueve la plasticidad bioenergética en el mieloma múltiple". Investigación sobre el cáncer . 79 (9): 2285–2297. doi : 10.1158/0008-5472.CAN-18-0773 . PMID 30622116.
- ^ Dagar S, Pathak D, Oza HV, Mylavarapu SV (noviembre de 2021). "Nanotubos de efecto túnel y estructuras relacionadas: mecanismos moleculares de formación y función". The Biochemical Journal . 478 (22): 3977–3998. doi :10.1042/bcj20210077. PMID 34813650. S2CID 244529025.
- ^ Ady JW, Desir S, Thayanithy V, Vogel RI, Moreira AL, Downey RJ, et al. (31 de octubre de 2014). "Comunicación intercelular en el mesotelioma pleural maligno: propiedades de los nanotubos tunelizadores". Frontiers in Physiology . 5 : 400. doi : 10.3389/fphys.2014.00400 . PMC 4215694 . PMID 25400582.
- ^ Saha T, Dash C, Jayabalan R, Khiste S, Kulkarni A, Kurmi K, et al. (enero de 2022). "Los nanotubos intercelulares median el tráfico mitocondrial entre las células cancerosas y las inmunes". Nature Nanotechnology . 17 (1): 98–106. Bibcode :2022NatNa..17...98S. doi :10.1038/s41565-021-01000-4. PMC 10071558 . PMID 34795441. S2CID 244349825.
- ^ Torralba D, Baixauli F, Sánchez-Madrid F (2016). "Las mitocondrias no conocen fronteras: mecanismos y funciones de la transferencia mitocondrial intercelular". Frontiers in Cell and Developmental Biology . 4 : 107. doi : 10.3389/fcell.2016.00107 . PMC 5039171 . PMID 27734015.
- ^ Wang X, Gerdes HH (julio de 2015). "La transferencia de mitocondrias a través de nanotubos de tunelización rescata células PC12 apoptóticas". Muerte celular y diferenciación . 22 (7): 1181–1191. doi :10.1038/cdd.2014.211. PMC 4572865 . PMID 25571977.
- ^ Pasquier J, Guerrouahen BS, Al Thawadi H, Ghiabi P, Maleki M, Abu-Kaoud N, et al. (abril de 2013). "La transferencia preferencial de mitocondrias desde células endoteliales a células cancerosas a través de nanotubos de efecto túnel modula la quimiorresistencia". Journal of Translational Medicine . 11 (1): 94. doi : 10.1186/1479-5876-11-94 . PMC 3668949 . PMID 23574623.
- ^ Lu J, Zheng X, Li F, Yu Y, Chen Z, Liu Z, et al. (febrero de 2017). "Los nanotubos de tunelización promueven la transferencia mitocondrial intercelular seguida de una mayor invasividad en las células del cáncer de vejiga". Oncotarget . 8 (9): 15539–15552. doi :10.18632/oncotarget.14695. PMC 5362504 . PMID 28107184.
- ^ Li X, Zhang Y, Yeung SC, Liang Y, Liang X, Ding Y, et al. (septiembre de 2014). "La transferencia mitocondrial de células madre mesenquimales derivadas de células madre pluripotentes inducidas a células epiteliales de las vías respiratorias atenúa el daño inducido por el humo del cigarrillo". American Journal of Respiratory Cell and Molecular Biology . 51 (3): 455–465. doi :10.1165/rcmb.2013-0529OC. PMID 24738760.
- ^ abcde Callier, Viviane (23 de abril de 2018). "Las células se comunican y se ayudan entre sí a través de pequeñas redes de tubos". Quanta Magazine . Consultado el 25 de septiembre de 2024 .
- ^ Smith IF, Shuai J, Parker I (abril de 2011). "Generación activa y propagación de señales de Ca2+ dentro de nanotubos de membrana de efecto túnel". Biophysical Journal . 100 (8): L37–L39. Bibcode :2011BpJ...100L..37S. doi :10.1016/j.bpj.2011.03.007. PMC 3077701 . PMID 21504718.
- ^ Kumar A, Kim JH, Ranjan P, Metcalfe MG, Cao W, Mishina M, et al. (enero de 2017). "El virus de la gripe explota los nanotubos de efecto túnel para propagarse de célula a célula". Scientific Reports . 7 (1): 40360. Bibcode :2017NatSR...740360K. doi :10.1038/srep40360. PMC 5216422 . PMID 28059146.
- ^ Jansens RJ, Tishchenko A, Favoreel HW (marzo de 2020). Glaunsinger BA (ed.). "Cerrando la brecha: propagación del virus a larga distancia mediante nanotubos de efecto túnel". Journal of Virology . 94 (8): e02120–19. doi :10.1128/JVI.02120-19. PMC 7108841 . PMID 32024778.
- ^ "El coronavirus puede entrar al cerebro construyendo pequeños túneles a través de la nariz". New Scientist . Consultado el 23 de agosto de 2022 .
- ^ Pepe A, Pietropaoli S, Vos M, Barba-Spaeth G, Zurzolo C (julio de 2022). "Los nanotubos de efecto túnel proporcionan una ruta para la propagación del SARS-CoV-2". Science Advances . 8 (29): eabo0171. Bibcode :2022SciA....8O.171P. doi : 10.1126/sciadv.abo0171 . PMC 9299553 . PMID 35857849.
- ^ Ottonelli I, Caraffi R, Tosi G, Vandelli MA, Duskey JT, Ruozi B (febrero de 2022). "Nanotubos de efecto túnel: ¿un nuevo objetivo para la nanomedicina?". Revista internacional de ciencias moleculares . 23 (4): 2237. doi : 10.3390/ijms23042237 . PMC 8878036 . PMID 35216348.
- ^ Gallagher KL, Benfey PN (enero de 2005). "No es solo otro agujero en la pared: comprensión del tráfico de proteínas intercelulares". Genes & Development . 19 (2): 189–195. doi : 10.1101/gad.1271005 . PMID 15655108.
- ^ Köhler RH, Cao J, Zipfel WR, Webb WW, Hanson MR (junio de 1997). "Intercambio de moléculas de proteína a través de conexiones entre plástidos de plantas superiores". Science . 276 (5321): 2039–2042. doi :10.1126/science.276.5321.2039. PMID 9197266.
- ^ Kuznetsov AV (agosto de 2011). "Modelado del transporte bidireccional de nanopartículas de puntos cuánticos en nanotubos de membrana". Ciencias biológicas matemáticas . 232 (2): 101–109. doi :10.1016/j.mbs.2011.04.008. PMID 21609723.
- ^ Rodríguez-Vázquez N, Fuertes A, Amorín M, Granja JR (2016). "Canales artificiales de iones de sodio y potasio bioinspirados". En Sigel A, Sigel H, Sigel RK (eds.). Los iones de metales alcalinos: su papel en la vida . Iones metálicos en ciencias biológicas. vol. 16. págs. 485–556. doi :10.1007/978-3-319-21756-7_14. ISBN 978-3-319-21755-0. Número de identificación personal 26860310.
Lectura adicional
- Gurke S, Barroso JF, Gerdes HH (mayo de 2008). "El arte de la comunicación celular: los nanotubos tunelados cierran la brecha". Histoquímica y biología celular . 129 (5): 539–550. doi :10.1007/s00418-008-0412-0. PMC 2323029 . PMID 18386044.
- "Nanotubos con efecto túnel: la red secreta de la vida". New Scientist . Noviembre de 2008.
Enlaces externos
- Grupo de investigación Hans-Hermann Gerdes: el laboratorio que observó por primera vez los nanotubos de membrana