Componente del ARN de la telomerasa
| TERC | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificadores | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Alias | TERC , DKCA1, PFBMFT2, SCARNA19, TR, TRC3, hTR, componente de ARN de telomerasa, TER | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificaciones externas | OMIM : 602322; Tarjetas genéticas : TERC; OMA :TERC - ortólogos | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidatos | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| ARN de la telomerasa de vertebrados | |
|---|---|
 | |
| Identificadores | |
| Símbolo | Telomerasa-vert |
| RFAM | RF00024 |
| Otros datos | |
| Tipo de ARN | Gene |
| Dominio(s) | Eucariota ; Virus |
| Estructuras del PDB | PDBe |
| ARN de la telomerasa ciliada | |
|---|---|
 | |
| Identificadores | |
| Símbolo | Telomerasa-cil |
| RFAM | RF00025 |
| Otros datos | |
| Tipo de ARN | Gene |
| Dominio(s) | Eucariota |
| Estructuras del PDB | PDBe |
| ARN de la telomerasa de Saccharomyces cerevisiae | |
|---|---|
 | |
| Identificadores | |
| Símbolo | Sacc_telomerasa |
| RFAM | RF01050 |
| Otros datos | |
| Tipo de ARN | Gene |
| Dominio(s) | Eucariota |
| Estructuras del PDB | PDBe |
El componente ARN de la telomerasa , también conocido como TR , TER o TERC , es un ARNnc que se encuentra en eucariotas y que es un componente de la telomerasa , la enzima utilizada para extender los telómeros . [3] [4] El TERC sirve como plantilla para la replicación de los telómeros ( transcripción inversa ) por la telomerasa. Los ARN de la telomerasa difieren mucho en secuencia y estructura entre vertebrados, ciliados y levaduras, pero comparten una estructura de pseudonudo 5' cercana a la secuencia de la plantilla. Los ARN de la telomerasa de vertebrados tienen un dominio 3' H/ACA similar al ARNsno . [5] [6] [7]
Estructura
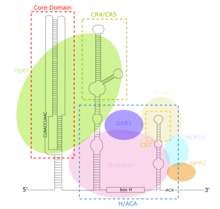
TERC es un ARN largo no codificante (lncRNA) que varía en longitud desde ~150 nt en ciliados hasta 400-600 nt en vertebrados y 1300 nt en levaduras (Alnafakh). El TERC humano maduro (hTR) tiene una longitud de 451 nt. [8] TERC tiene amplias características estructurales secundarias en 4 dominios principales conservados. [9] El dominio central, el dominio más grande en el extremo 5' de TERC, contiene la secuencia de plantilla de telómero CUAAC . Su estructura secundaria consiste en un gran bucle que contiene la secuencia de plantilla, una hélice de cierre de bucle P1 y un pseudonudo P2/P3 . [10] El dominio central y el dominio conservado CR4/CR5 se asocian con TERT y son los únicos dominios de TERC necesarios para la actividad catalítica in vitro de la telomerasa. [11] El extremo 3' de TERC consiste en un dominio H/ACA conservado, [10] una estructura de 2 horquillas conectadas por una bisagra monocatenaria y bordeada en el extremo 3' por una secuencia ACA monocatenaria. [8] El dominio H/ACA se une a Dyskerin , GAR1 , NOP10, NHP2 , para formar un complejo H/ACA RNP . [10] El dominio CR7 conservado también está localizado en el extremo 3' de TERC, y contiene una caja CAB ( Cajal body Localisation) de 3 nt que se une a TCAB1. [10]
Función
La telomerasa es una polimerasa de ribonucleoproteína que mantiene los extremos de los telómeros mediante la adición de la repetición de telómero TTAGGG. Esta repetición varía entre eucariotas (consulte la tabla en el artículo sobre los telómeros para obtener una lista completa). La enzima consta de un componente proteico ( TERT ) con actividad de transcriptasa inversa y un componente de ARN, codificado por este gen, que sirve como plantilla para la repetición de telómero. La CCCUAA, que se encuentra cerca de la posición 50 de la secuencia TERC de vertebrados, actúa como plantilla. La expresión de la telomerasa desempeña un papel en la senescencia celular , ya que normalmente se reprime en las células somáticas posnatales , lo que da como resultado un acortamiento progresivo de los telómeros. La desregulación de la expresión de la telomerasa en las células somáticas puede estar involucrada en la oncogénesis . Los estudios en ratones sugieren que la telomerasa también participa en la reparación cromosómica , ya que la síntesis de novo de repeticiones de telómeros puede ocurrir en roturas de doble cadena . [12] También se pueden encontrar homólogos de TERC en los virus del herpes zóster . [13]
El dominio central de TERC contiene la plantilla de ARN a partir de la cual TERT sintetiza repeticiones teloméricas TTAGGG. [10] A diferencia de otras RNP, en la telomerasa , la proteína TERT es catalítica mientras que el lncRNA TERC es estructural, en lugar de actuar como una ribozima . [14] La región central de TERC y TERT son suficientes para reconstituir la actividad catalítica de la telomerasa in vitro. [10] [11] El dominio H/ACA de TERC recluta el complejo disquerina ( DKC1 , GAR1 , NOP10, NHP2 ), que estabiliza TERC, aumentando la formación del complejo de telomerasa y la actividad catalítica general. [10] El dominio CR7 se une a TCAB1, que localiza la telomerasa en los cuerpos de Cajal , aumentando aún más la actividad catalítica de la telomerasa. [10] TERC se expresa de forma ubicua, incluso en células que carecen de actividad de telomerasa y expresión de TERT. [15] Como resultado, se han propuesto varios papeles funcionales independientes de TERT de TERC. 14 genes que contienen un motivo de unión de TERC están regulados transcripcionalmente directamente por TERC a través del aumento de la expresión mediado por la formación de tripletes ARN-ADN. La regulación positiva mediada por TERC de Lin37, Trpg1l, tyrobp , Usp16 estimula la vía NF-κB , lo que resulta en un aumento de la expresión y secreción de citocinas inflamatorias . [16]
Biosíntesis
A diferencia de la mayoría de los lncRNA que se ensamblan a partir de intrones por el espliceosoma , el hTR se transcribe directamente desde un sitio promotor dedicado [8] ubicado en el locus genómico 3q26.2 [17] por la ARN polimerasa II . [8] El hTR maduro tiene una longitud de 451 nt, pero aproximadamente 1/3 de las transcripciones de hTR celulares en estado estable tienen colas 3' codificadas genómicamente de ~10 nt. La mayoría de esas especies de hTR extendidas tienen una extensión 3' oligo-A adicional. [8] El procesamiento del hTR inmaduro con cola 3' a hTR maduro de 451 nt se puede lograr mediante degradación exorribonucleolítica 3'-5' directa o mediante una vía indirecta de oligoadenilación por PAPD5, eliminación de la cola 3' oligo-A por la exonucleasa de ARN 3'-5' PARN y posterior degradación exorribonucleolítica 3'-5'. [8] Las transcripciones hTR extendidas también son degradadas por el exosoma de ARN . [8]
Los extremos 5' de las transcripciones de hTR también se procesan adicionalmente. TGS-1 hipermetila la tapa de 5'-metilguanosina a una tapa de N2,2,7 trimetilguanosina (TMG), que inhibe la maduración de hTR. [18] La unión del complejo de disquerina a los dominios H/ACA transcritos de hTR durante la transcripción promueve la terminación de la transcripción. [8] El control de las tasas relativas de estas diversas vías competitivas que activan o inhiben la maduración de hTR es un elemento crucial de la regulación de la actividad general de la telomerasa.
Importancia clínica
Las mutaciones de pérdida de función en el locus genómico TERC se han asociado con una variedad de enfermedades degenerativas . Las mutaciones en TERC se han asociado con disqueratosis congénita , [19] fibrosis pulmonar idiopática , [20] anemia aplásica y mielodisplasia . [10] La sobreexpresión y regulación inadecuada de TERC se han asociado con una variedad de cánceres . La regulación positiva de hTR se observa ampliamente en pacientes con fenotipo cervical precanceroso como resultado de la infección por VPH . [21] La sobreexpresión de TERC mejora la oncogénesis mediada por MDV , [22] y se observa en el carcinoma gástrico . [23] La sobreexpresión de TERC también se observa en condiciones inflamatorias como diabetes tipo II y esclerosis múltiple , debido a la activación mediada por TERC de la vía inflamatoria NF-κB . [16]
Se ha implicado a TERC como protector en la osteoporosis , y su mayor expresión detiene la tasa de osteogénesis . [24] Debido a su sobreexpresión en una variedad de fenotipos de cáncer, se ha investigado a TERC como un posible biomarcador del cáncer . Se descubrió que es un biomarcador eficaz del carcinoma de células escamosas de pulmón (LUSC). [25]
Referencias
- ^ abc GRCh38: Lanzamiento de Ensembl 89: ENSG00000277925 – Ensembl , mayo de 2017
- ^ "Referencia de PubMed humana:". Centro Nacional de Información Biotecnológica, Biblioteca Nacional de Medicina de EE. UU .
- ^ Feng J, Funk WD, Wang SS, Weinrich SL, Avilion AA, Chiu CP, et al. (septiembre de 1995). "El componente ARN de la telomerasa humana". Science . 269 (5228): 1236–41. Bibcode :1995Sci...269.1236F. doi :10.1126/science.7544491. PMID 7544491. S2CID 9440710.
- ^ Jády BE, Richard P, Bertrand E, Kiss T (febrero de 2006). "Reclutamiento dependiente del ciclo celular de ARN de la telomerasa y cuerpos de Cajal a telómeros humanos". Biología molecular de la célula . 17 (2): 944–54. doi :10.1091/mbc.E05-09-0904. PMC 1356602 . PMID 16319170.
- ^ McCormick-Graham M, Romero DP (abril de 1995). "Características estructurales del ARN de la telomerasa ciliada". Nucleic Acids Research . 23 (7): 1091–7. doi :10.1093/nar/23.7.1091. PMC 306816 . PMID 7739888.
- ^ Lingner J, Hendrick LL, Cech TR (agosto de 1994). "Los ARN de la telomerasa de diferentes ciliados tienen una estructura secundaria común y una plantilla permutada". Genes & Development . 8 (16): 1984–98. doi : 10.1101/gad.8.16.1984 . PMID 7958872.
- ^ Theimer CA, Feigon J (junio de 2006). "Estructura y función del ARN de la telomerasa". Current Opinion in Structural Biology . 16 (3): 307–18. doi :10.1016/j.sbi.2006.05.005. PMID 16713250.
- ^ abcdefgh Roake CM, Chen L, Chakravarthy AL, Ferrell JE, Raffa GD, Artandi SE (mayo de 2019). "La alteración de la cinética de maduración del ARN de la telomerasa precipita la enfermedad". Molecular Cell . 74 (4): 688–700.e3. doi :10.1016/j.molcel.2019.02.033. PMC 6525023 . PMID 30930056.
- ^ Alnafakh RA, Adishesh M, Button L, Saretzki G, Hapangama DK (2019). "Telomerasa y telómeros en el cáncer de endometrio". Frontiers in Oncology . 9 : 344. doi : 10.3389/fonc.2019.00344 . PMC 6533802 . PMID 31157162.
- ^ abcdefghi Zhang Q, Kim NK, Feigon J (diciembre de 2011). "Arquitectura del ARN de la telomerasa humana". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 108 (51): 20325–32. Bibcode :2011PNAS..10820325Z. doi : 10.1073/pnas.1100279108 . PMC 3251123 . PMID 21844345.
- ^ ab Webb CJ, Zakian VA (agosto de 2016). "El ARN de la telomerasa es más que una plantilla de ADN". RNA Biology . 13 (8): 683–9. doi :10.1080/15476286.2016.1191725. PMC 4993324 . PMID 27245259.
- ^ "Gen Entrez: componente ARN de la telomerasa TERC".
- ^ Fragnet L, Kut E, Rasschaert D (junio de 2005). "Estudio funcional comparativo del ARN de la telomerasa viral basado en mutaciones naturales". The Journal of Biological Chemistry . 280 (25): 23502–15. doi : 10.1074/jbc.M501163200 . PMID 15811851. S2CID 24301693.
- ^ Wang Y, Sušac L, Feigon J (diciembre de 2019). "Biología estructural de la telomerasa". Cold Spring Harbor Perspectives in Biology . 11 (12): a032383. doi :10.1101/cshperspect.a032383. PMC 6886448 . PMID 31451513.
- ^ Shay JW, Wright WE (mayo de 2019). "Telómeros y telomerasa: tres décadas de progreso". Nature Reviews Genetics . 20 (5): 299–309. doi :10.1038/s41576-019-0099-1. PMID 30760854. S2CID 61156603.
- ^ ab Liu H, Yang Y, Ge Y, Liu J, Zhao Y (septiembre de 2019). "TERC promueve la respuesta inflamatoria celular independiente de la telomerasa". Investigación de ácidos nucleicos . 47 (15): 8084–8095. doi : 10.1093/nar/gkz584. PMC 6735767 . PMID 31294790.
- ^ "Entrada OMIM - * 602322 - COMPONENTE ARN DE LA TELOMERASA; TERC". www.omim.org . Consultado el 2 de marzo de 2020 .
- ^ Chen L, Roake CM, Galati A, Bavasso F, Micheli E, Saggio I, et al. (febrero de 2020). "La pérdida de la hipermetilasa TGS1 humana promueve el aumento de la elongación del ARN de la telomerasa y de los telómeros". Cell Reports . 30 (5): 1358–1372.e5. doi :10.1016/j.celrep.2020.01.004. PMC 7156301 . PMID 32023455.
- ^ Rich RR (13 de enero de 2018). Inmunología clínica: principios y práctica (Quinta edición). [St. Louis, Mo.] ISBN 978-0-7020-7039-6.OCLC 1023865227 .
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) - ^ Swigris JJ, Brown KK (25 de julio de 2018). Fibrosis pulmonar idiopática . St. Louis. ISBN 978-0-323-54432-0.OCLC 1053744041 .
{{cite book}}: CS1 maint: location missing publisher (link) - ^ Liu Y, Fan P, Yang Y, Xu C, Huang Y, Li D, et al. (noviembre de 2019). "El virus del papiloma humano y el gen componente del ARN de la telomerasa humana en la progresión del cáncer de cuello uterino". Informes científicos . 9 (1): 15926. Código bibliográfico : 2019NatSR...915926L. doi :10.1038/s41598-019-52195-5. PMC 6828729 . PMID 31685833.
- ^ Kheimar A, Trimpert J, Groenke N, Kaufer BB (marzo de 2019). "La sobreexpresión del ARN de la telomerasa celular mejora la formación de cáncer inducida por virus". Oncogene . 38 (10): 1778–1786. doi :10.1038/s41388-018-0544-1. PMID 30846849. S2CID 53085869.
- ^ Heine B, Hummel M, Demel G, Stein H (junio de 1998). "Demostración de una regulación positiva constante del componente ARN de la telomerasa en carcinomas gástricos humanos mediante hibridación in situ". The Journal of Pathology . 185 (2): 139–44. doi :10.1002/(SICI)1096-9896(199806)185:2<139::AID-PATH79>3.0.CO;2-L. PMID 9713339. S2CID 21966828.
- ^ Gao GC, Yang DW, Liu W (enero de 2020). "El lncRNA TERC alivia la progresión de la osteoporosis al absorber el miRNA-217 para regular positivamente RUNX2". Revista Europea de Ciencias Médicas y Farmacológicas . 24 (2): 526–534. doi :10.26355/eurrev_202001_20029. PMID 32016954. S2CID 211024218.
- ^ Storti CB, de Oliveira RA, de Carvalho M, Hasimoto EN, Cataneo DC, Cataneo AJ, et al. (febrero de 2020). "Los genes asociados a los telómeros y los lncRNA teloméricos son candidatos a biomarcadores en el carcinoma de células escamosas de pulmón (LUSC)". Experimental and Molecular Pathology . 112 : 104354. doi :10.1016/j.yexmp.2019.104354. PMID 31837325. S2CID 209385638.
Lectura adicional
- de Lange T, Jacks T (agosto de 1999). "¿Para bien o para mal? Inhibición de la telomerasa y cáncer". Cell . 98 (3): 273–5. doi : 10.1016/S0092-8674(00)81955-8 . PMID 10458601. S2CID 14642341.
- Marrone A, Dokal I (diciembre de 2004). "Disqueratosis congénita: perspectivas moleculares sobre la función de la telomerasa, el envejecimiento y el cáncer". Expert Reviews in Molecular Medicine . 6 (26): 1–23. doi :10.1017/S1462399404008671. PMID 15613268. S2CID 38163343.
- Yamaguchi H (junio de 2007). "Mutaciones de genes del complejo de la telomerasa vinculadas a fallas de la médula ósea". Journal of Nippon Medical School . 74 (3): 202–9. doi : 10.1272/jnms.74.202 . PMID 17625368.
- Zaug AJ, Linger J, Cech TR (febrero de 1996). "Método para determinar los extremos 3' del ARN y aplicación al ARN de la telomerasa humana". Nucleic Acids Research . 24 (3): 532–3. doi :10.1093/nar/24.3.532. PMC 145649 . PMID 8602368.
- Soder AI, Hoare SF, Muire S, Balmain A, Parkinson EK, Keith WN (abril de 1997). "Mapeo del gen del componente de ARN de la telomerasa de ratón, Terc, en el cromosoma 3 mediante hibridación in situ con fluorescencia y pintura cromosómica de ratón". Genomics . 41 (2): 293–4. doi :10.1006/geno.1997.4621. PMID 9143511.
- Zhao JQ, Hoare SF, McFarlane R, Muir S, Parkinson EK, Black DM, Keith WN (marzo de 1998). "Clonación y caracterización de secuencias promotoras del gen ARN de la telomerasa humana y de ratón". Oncogene . 16 (10): 1345–50. doi :10.1038/sj.onc.1201892. PMID 9546436. S2CID 2699389.
- Mitchell JR, Wood E, Collins K (diciembre de 1999). "Un componente de la telomerasa es defectuoso en la enfermedad humana disqueratosis congénita". Nature . 402 (6761): 551–5. Bibcode :1999Natur.402..551M. doi :10.1038/990141. PMID 10591218. S2CID 4430482.
- Chen JL, Blasco MA, Greider CW (marzo de 2000). "Estructura secundaria del ARN de la telomerasa de vertebrados". Cell . 100 (5): 503–14. doi : 10.1016/S0092-8674(00)80687-X . PMID 10721988. S2CID 15642776.
- Wong KK, Chang S, Weiler SR, Ganesan S, Chaudhuri J, Zhu C, et al. (septiembre de 2000). "La disfunción de los telómeros afecta la reparación del ADN y aumenta la sensibilidad a la radiación ionizante". Nature Genetics . 26 (1): 85–8. doi :10.1038/79232. PMID 10973255. S2CID 1873111.
- Mitchell JR, Collins K (agosto de 2000). "La activación de la telomerasa humana requiere dos interacciones independientes entre el ARN de la telomerasa y la transcriptasa inversa de la telomerasa". Molecular Cell . 6 (2): 361–71. doi : 10.1016/S1097-2765(00)00036-8 . PMID 10983983.
- Imoto I, Pimkhaokham A, Fukuda Y, Yang ZQ, Shimada Y, Nomura N, et al. (agosto de 2001). "SNO es un objetivo probable para la amplificación génica en 3q26 en carcinomas de células escamosas del esófago". Comunicaciones de investigación bioquímica y biofísica . 286 (3): 559–65. doi :10.1006/bbrc.2001.5428. PMID 11511096.
- Vulliamy T, Marrone A, Goldman F, Dearlove A, Bessler M, Mason PJ, Dokal I (septiembre de 2001). "El componente ARN de la telomerasa está mutado en la disqueratosis congénita autosómica dominante". Nature . 413 (6854): 432–5. Bibcode :2001Natur.413..432V. doi :10.1038/35096585. PMID 11574891. S2CID 4348062.
- Pruzan R, Pongracz K, Gietzen K, Wallweber G, Gryaznov S (enero de 2002). "Inhibidores alostéricos de la telomerasa: oligonucleótidos N3'-->P5' fosforamidatos". Nucleic Acids Research . 30 (2): 559–68. doi :10.1093/nar/30.2.559. PMC 99832 . PMID 11788719.
- Zhang RG, Zhang RP, Wang XW, Xie H (marzo de 2002). "Efectos del cisplatino en la actividad de la telomerasa y la longitud de los telómeros en células de hepatoma humano BEL-7404". Cell Research . 12 (1): 55–62. doi : 10.1038/sj.cr.7290110 . PMID 11942411. S2CID 36839452.
- Yang Y, Chen Y, Zhang C, Huang H, Weissman SM (julio de 2002). "La localización nucleolar de la proteína hTERT está asociada con la función de la telomerasa". Experimental Cell Research . 277 (2): 201–9. doi :10.1006/excr.2002.5541. PMID 12083802.
- Chang JT, Chen YL, Yang HT, Chen CY, Cheng AJ (julio de 2002). "Regulación diferencial de la actividad de la telomerasa por seis subunidades de la telomerasa". Revista Europea de Bioquímica . 269 (14): 3442–50. doi : 10.1046/j.1432-1033.2002.03025.x . PMID 12135483.
- Gavory G, Farrow M, Balasubramanian S (octubre de 2002). "Requisito de longitud mínima del dominio de alineación del ARN de la telomerasa humana para mantener la actividad catalítica in vitro". Nucleic Acids Research . 30 (20): 4470–80. doi :10.1093/nar/gkf575. PMC 137139 . PMID 12384594.
- Sood AK, Coffin J, Jabbari S, Buller RE, Hendrix MJ, Klingelhutz A (2003). "Las mutaciones nulas de p53 se asocian con un fenotipo negativo para la telomerasa en el carcinoma de ovario". Cancer Biology & Therapy . 1 (5): 511–7. doi : 10.4161/cbt.1.5.167 . PMID 12496479. S2CID 45381814.
- Antal M, Boros E, Solymosy F, Kiss T (febrero de 2002). "Análisis de la estructura del ARN de la telomerasa humana in vivo". Nucleic Acids Research . 30 (4): 912–20. doi :10.1093/nar/30.4.912. PMC 100349 . PMID 11842102.
Enlaces externos
- Entrada de GeneReviews/NCBI/NIH/UW sobre disqueratosis congénita
- Entrada de GeneReviews/NCBI/NIH/UW sobre fibrosis pulmonar familiar
- Página de EntrezGene para TERC
- Página sobre el ARN de la telomerasa de vertebrados en Rfam
- Página de ARN de la telomerasa ciliada en Rfam
- Página de la telomerasa de Saccharomyces en Rfam



