Modulador selectivo del receptor de glucocorticoides
| Modulador selectivo del receptor de glucocorticoides | |
|---|---|
| Clase de droga | |
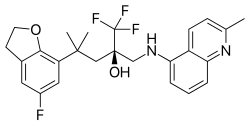 Estructura química del mapracorat , uno de los SEGRA más desarrollados. [1] | |
| Identificadores de clase | |
| Sinónimos | SEGRM; SEGRA; SEGRAM; DIGRA |
| Usar | Posible dermatitis atópica , glaucoma , cataratas , infecciones oculares y otras. |
| Objetivo biológico | Receptor de glucocorticoides |
| Clase química | Esteroideo ; no esteroide |
| Estatus legal | |
| En Wikidata | |
Los moduladores selectivos del receptor de glucocorticoides ( SEGRM ) y los agonistas selectivos del receptor de glucocorticoides ( SEGRA ), anteriormente conocidos como agonistas del receptor de glucocorticoides disociados ( DIGRA ), son una clase de fármacos experimentales diseñados para compartir muchas de las propiedades antiinflamatorias , inmunosupresoras o anticancerígenas deseables de los fármacos glucocorticoides clásicos , pero con menos efectos secundarios como la atrofia de la piel . Aunque la evidencia preclínica sobre los efectos antiinflamatorios de los SEGRAM está culminando, [2] actualmente, la eficacia de estos SEGRAM en el cáncer es en gran parte desconocida.
Los agonistas selectivos del receptor de glucocorticoides (SEGRA) tienen una estructura típicamente esteroidea, mientras que los moduladores selectivos del receptor de glucocorticoides (SEGRM) son típicamente no esteroideos . La abreviatura combinada de agonista y modulador selectivo del receptor de glucocorticoides es SEGRAM . [2] Se han desarrollado varios de estos ligandos y se están evaluando en pruebas preclínicas y clínicas.
Los SEGRAM logran su selectividad al activar solo un subconjunto de los mecanismos de acción del receptor de glucocorticoides . [3] [4]
Historia
Los esteroides sintéticos con propiedades similares a las de SEGRA ya se descubrieron a finales de los años 1990. [5] Durante la década de 2000, se sintetizaron muchos SEGRAM potenciales, la mayoría de ellos con estructuras no esteroideas. En estudios in vitro en modelos celulares , estas moléculas SEGRAM se unen al receptor de glucocorticoides con una afinidad similar a la dexametasona , un potente glucocorticoide, y con una capacidad para reprimir la producción de mediadores inflamatorios como la interleucina 6 y la prostaglandina E2 . [6] Además, in vitro , un SEGRAM particular puede promover la apoptosis en el cáncer de próstata [7] y la leucemia . [8]
Estudios in vivo en ratones y ratas mostraron que un SEGRAM administrado tópicamente inhibió la actividad de la peroxidasa y la formación de edema , ambos indicadores de actividad antiinflamatoria, comparablemente a la prednisolona . La administración sistémica en ratones o ratas indica que los SEGRAM pueden disminuir las infecciones agudas , la artritis reumatoide , el asma y la colitis . [2] Actualmente falta evidencia in vivo sobre si los SEGRAM particulares pueden provocar efectos similares a los glucocorticoides clásicos en patologías cancerosas. Las pruebas preclínicas actuales muestran que los SEGRAM disponibles hasta ahora provocarían menos efectos secundarios o al menos efectos secundarios menos graves que los glucocorticoides clásicos. [2] Por ejemplo, la atrofia de la piel en ratas fue significativamente menos pronunciada que con prednisolona en un estudio utilizando el SEGRAM Mapracorat , y los efectos metabólicos como el aumento de peso o el aumento de la glucosa en sangre fueron prácticamente inexistentes. [9]
Mecanismo de acción

Tanto los glucocorticoides no selectivos como los agonistas selectivos del receptor de glucocorticoides actúan uniéndose al receptor de glucocorticoides (GR) y activándolo. A diferencia de los glucocorticoides, que activan el GR para que actúe a través de (al menos) dos vías de transducción de señales , [10] las SEGRAM activan el GR de tal manera que sólo actúa a través de una de las dos vías principales posibles. [11]
En ausencia de glucocorticoides, el GR reside en el citosol en un estado inactivo en un complejo con proteínas de choque térmico (HSP) e inmunofilinas . La unión de los glucocorticoides al GR activa el receptor al provocar un cambio conformacional en el GR y, por lo tanto, una disociación de las HSP unidas. El GR activado puede entonces regular la expresión génica a través de una de dos vías: [10]
- Transactivación
- La primera vía (directa) se denomina transactivación , mediante la cual el GR activado se dimeriza , se transloca al núcleo y se une a secuencias específicas de ADN llamadas elementos de respuesta a glucocorticoides (GRE). El complejo GR/ADN recluta otras proteínas que transcriben el ADN corriente abajo en ARNm y, finalmente, proteína . Algunos ejemplos de genes que responden a los glucocorticoides incluyen aquellos que codifican la anexina A1 , TSC22D3 (también conocida como GILZ), la enzima convertidora de angiotensina , la endopeptidasa neutra y otras proteínas antiinflamatorias.
- Transrepresión
- La segunda vía (indirecta) se denomina transrepresión , en la que el GR monomérico activado se une a otros factores de transcripción como NF-κB y AP-1 y evita que estos regulen positivamente la expresión de sus genes diana. Estos genes diana codifican proteínas como la ciclooxigenasa , la NO sintasa , la fosfolipasa A2 , el factor de necrosis tumoral , el factor de crecimiento transformante beta , ICAM-1 y varias otras proteínas proinflamatorias.

Por lo tanto, los efectos antiinflamatorios de los glucocorticoides resultan tanto de la transactivación como de la transrepresión. Por el contrario, los estudios en ratas y ratones han demostrado que la mayoría de los efectos secundarios de los glucocorticoides, como la actividad diabetogénica , la osteoporosis y la atrofia cutánea, son causados principalmente por la transactivación. [9] [12] [13] Un glucocorticoide selectivo que sea capaz de transreprimir sin transactivación debería preservar muchos de los efectos antiinflamatorios terapéuticos deseables y minimizar estos efectos secundarios no deseados en particular. [11]
La evidencia inicial de que la transpresión por sí sola puede ser suficiente para una respuesta antiinflamatoria fue proporcionada por la introducción de una mutación puntual en el GR de ratones que impidió que el GR dimerizara y se uniera al ADN y, por lo tanto, bloqueó la transactivación. [14] [15] Al mismo tiempo, esta mutación no interfirió con la transrepresión. Si bien el GR es esencial para la supervivencia, estos ratones aún son viables. [14] Sin embargo, cuando estos ratones fueron tratados con el glucocorticoide sintético dexametasona, no hubo elevación de la glucosa. Estos ratones tratados con dexametasona fueron resistentes a un estímulo inflamatorio. [15] Por lo tanto, estos ratones respondieron a los efectos antiinflamatorios de la dexametasona, pero fueron resistentes al menos a algunos de los efectos secundarios.
Al igual que los glucocorticoides, las SEGRAM se unen a los GR y los activan. Sin embargo, a diferencia de los glucocorticoides, las SEGRAM activan selectivamente los GR de tal manera que producen un beneficio terapéutico mejorado. En general, para enfermedades específicas basadas en la inflamación, las SEGRAM deberían transreprimir con mayor fuerza que transactivar, o mejor aún, solo transreprimir y no transactivar. Este tipo de activación selectiva de los GR debería dar como resultado menos efectos secundarios que los efectos secundarios esperados que aparecen con un tratamiento crónico con glucocorticoides clásicos. [16]
Ensayos clínicos
Los ensayos clínicos de fase II con uno de los compuestos candidatos, mapracorat (nombres de código BOL-303242-X y ZK 245186 [17] ), comenzaron en el verano de 2009. Uno fue un estudio de búsqueda de dosis doble ciego para un ungüento contra la dermatitis atópica realizado por Intendis, una parte de Bayer HealthCare Pharmaceuticals especializada en dermatología . [18] Un ensayo de fase III comenzó en noviembre de 2010, evaluando una suspensión oftálmica para el tratamiento de la inflamación después de la cirugía de cataratas, realizado por Bausch & Lomb . [19]
En 2011, Pfizer inició un ensayo de fase II con otro glucocorticoide disociado , fosdagrocorat (PF-04171327) (un profármaco de éster de fosfato de dagrocorat (PF-00251802) [20] [21] ), para la artritis reumatoide . [22]
Los resultados de estos ensayos clínicos aún no han sido revelados y todavía no se ha aprobado ningún SEGRAM para uso clínico.
Aplicaciones potenciales
En enfermedades inflamatorias crónicas como la dermatitis atópica (piel), la artritis reumatoide (articulaciones),..., los efectos secundarios de los corticosteroides son problemáticos debido al tratamiento a largo plazo necesario. Por ello, se están investigando los SEGRAM como tratamiento tópico alternativo. El tratamiento sistémico a largo plazo de las inflamaciones con corticosteroides es especialmente propenso a causar efectos secundarios metabólicos, lo que hace que el desarrollo de SEGRAM orales sea un objetivo interesante. [23] Queda por ver si los agonistas o moduladores selectivos de los receptores causan de hecho significativamente menos efectos secundarios que los corticoides clásicos en aplicaciones clínicas.
Efectos atróficos beneficiosos
Cabe destacar que los efectos atróficos de los glucocorticoides no siempre son una desventaja. El tratamiento de enfermedades hiperproliferativas como la psoriasis hace uso de esta propiedad. [24] Los SEGRAM probablemente serían menos efectivos en tales condiciones. Los avances recientes han demostrado que el primer esfuerzo hacia una separación total de la transrepresión y transactivación de GR mediante el uso de SEGRAM merece ser matizado ya que los genes antiinflamatorios estimulados por la transactivación de GR, como GILZ y DUSP1 , parecen desempeñar un papel importante. [25] [26] Sin embargo, la naturaleza más selectiva de estos SEGRAM aún reduciría el número de efectos secundarios mediados por GR y merece más pruebas clínicas.
Química


Los primeros SEGRA eran esteroides sintéticos. Un ejemplo es el RU 24858, uno de los primeros compuestos de este tipo que se publicaron. [5] Muchos SEGRA más nuevos tienen una estructura diferente, aunque la similitud con los esteroides todavía se puede ver en moléculas como la benzopiranoquinolina A 276575 o en derivados del octahidrofenantreno-2,7-diol. Se ha demostrado que todos estos compuestos exhiben propiedades SEGRA en modelos celulares o animales. [3]
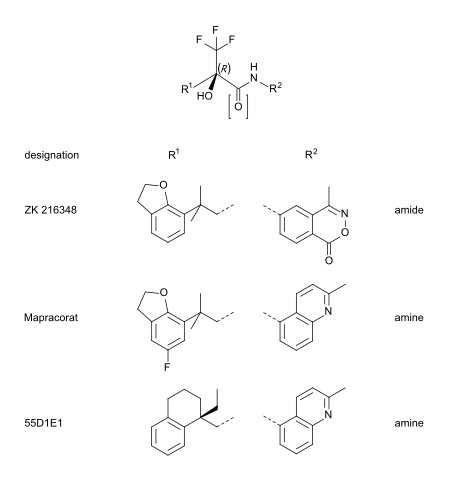
El mapracorat es una de las trifluoropropanolaminas y amidas que tienen una estructura menos obviamente similar a la de los esteroides. Otros ejemplos típicos de este grupo son ZK 216348 [9] y 55D1E1. [4] Los sustituyentes aromáticos bicíclicos y voluminosos (R 1 y R 2 ) explican la similitud estructural con los corticoides. La conformación R del átomo de carbono asimétrico parece ser esencial para la afinidad por los RG. [9]
Lista de SEGRM
- Dagrocorat (PF-00251802, PF-251802)
- Fosdagrocorat (PF-04171327, PF-4171327)
- Maparacorat (BOL-303242-X, ZK-245186)
Véase también
- Modulador selectivo del receptor
- Modulador selectivo del receptor de andrógenos
- Modulador selectivo del receptor de estrógeno
- Modulador selectivo del receptor de progesterona
Referencias
- ^ Harinoso N; Dulsat C (2009). "36ª Reunión Anual de la Arbeitsgemeinschaft Dermatologische Forschung (ADF)". Drogas Fut . 34 (4): 341.
- ^ abcd Sundahl N, Bridelance J, Libert C, De Bosscher K, Beck IM (mayo de 2015). "Modulación selectiva del receptor de glucocorticoides: nuevas direcciones con estructuras no esteroideas". Farmacología y terapéutica . 152 : 28–41. doi : 10.1016/j.pharmthera.2015.05.001 . hdl : 1854/LU-6896362 . PMID 25958032.
- ^ abc Robinson RP, Buckbinder L, Haugeto AI, McNiff PA, Millham ML, Reese MR, Schaefer JF, Abramov YA, Bordner J, Chantigny YA, Kleinman EF, Laird ER, Morgan BP, Murray JC, Salter ED, Wessel MD, Yocum SA (marzo de 2009). "Análogos de octahidrofenantreno-2,7-diol como agonistas del receptor de glucocorticoides disociados: descubrimiento y exploración de pistas". Journal of Medicinal Chemistry . 52 (6): 1731–43. doi :10.1021/jm801512v. PMID 19239259.
- ^ ab Biggadike K, Boudjelal M, Clackers M, Coe DM, Demaine DA, Hardy GW, Humphreys D, Inglis GG, Johnston MJ, Jones HT, House D, Loiseau R, Needham D, Skone PA, Uings I, Veitch G, Weingarten GG, McLay IM, Macdonald SJ (diciembre de 2007). "Agonistas de glucocorticoides no esteroides: tetrahidronaftalenos con miméticos de anillo A esteroides alternativos que poseen selectividad de eficacia disociada (transrepresión/transactivación)". Journal of Medicinal Chemistry . 50 (26): 6519–34. doi :10.1021/jm070778w. PMID 18038970.
- ^ abc Vayssière BM, Dupont S, Choquart A, Petit F, Garcia T, Marchandeau C, Gronemeyer H, Resche-Rigon M (agosto de 1997). "Los glucocorticoides sintéticos que disocian la transactivación y la transrepresión de AP-1 exhiben actividad antiinflamatoria in vivo". Endocrinología molecular . 11 (9): 1245–55. doi : 10.1210/mend.11.9.9979 . PMID 9259316. S2CID 28436574.
- ^ ab Lin CW, Nakane M, Stashko M, Falls D, Kuk J, Miller L, Huang R, Tyree C, Miner JN, Rosen J, Kym PR, Coghlan MJ, Carter G, Lane BC (agosto de 2002). "Propiedades de transactivación y represión del nuevo ligando del receptor de glucocorticoides no esteroides 2,5-dihidro-9-hidroxi-10-metoxi-2,2,4-trimetil-5-(1-metilciclohexen-3-il)-1H-[1]benzopirano[3,4-f]quinolina (A276575) y sus cuatro estereoisómeros". Farmacología molecular . 62 (2): 297–303. doi :10.1124/mol.62.2.297. PMID 12130681.
- ^ Yemelyanov A, Czwornog J, Gera L, Joshi S, Chatterton RT, Budunova I (junio de 2008). "Un nuevo compuesto fitomodulador del receptor de esteroides a inhibe el crecimiento y la supervivencia de las células del cáncer de próstata". Cancer Research . 68 (12): 4763–73. doi :10.1158/0008-5472.CAN-07-6104. PMID 18559523.
- ^ Lesovaya EA, Yemelyanov AY, Kirsanov KI, Yakubovskaya MG, Budunova IV (noviembre de 2011). "Efecto antitumoral del ligando del receptor de glucocorticoides no esteroideos CpdA en las líneas celulares de leucemia CEM y K562" (PDF) . Bioquímica. Biokhimiia . 76 (11): 1242–52. doi :10.1134/S000629791111006X. PMID 22117551. S2CID 35234449. Archivado desde el original (PDF) el 2016-03-11 . Consultado el 2015-05-28 .
- ^ abcd Schäcke H, Schottelius A, Döcke WD, Strehlke P, Jaroch S, Schmees N, Rehwinkel H, Hennekes H, Asadullah K (enero de 2004). "La disociación de la transactivación de la transrepresión por un agonista selectivo del receptor de glucocorticoides conduce a la separación de los efectos terapéuticos de los efectos secundarios". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 101 (1): 227–32. Bibcode :2004PNAS..101..227S. doi : 10.1073/pnas.0300372101 . PMC 314167 . PMID 14694204.
- ^ ab Rhen T, Cidlowski JA (octubre de 2005). "Acción antiinflamatoria de los glucocorticoides: nuevos mecanismos para fármacos antiguos". The New England Journal of Medicine . 353 (16): 1711–23. doi :10.1056/NEJMra050541. PMID 16236742. S2CID 5744727.
- ^ ab Newton R, Holden NS (octubre de 2007). "Separación de la transrepresión y la transactivación: ¿un divorcio angustiante para el receptor de glucocorticoides?". Farmacología molecular . 72 (4): 799–809. doi :10.1124/mol.107.038794. PMID 17622575. S2CID 52803631.
- ^ Heinemann A, Schuligoi R (2008). "Glucocorticoide – potente und umstritten" [Glucocorticoides – potente y controvertido]. Österreichische Apothekerzeitung (en alemán). 62 (23).[ enlace muerto permanente ]
- ^ Coghlan MJ, Jacobson PB, Lane B, Nakane M, Lin CW, Elmore SW, Kym PR, Luly JR, Carter GW, Turner R, Tyree CM, Hu J, Elgort M, Rosen J, Miner JN (mayo de 2003). "Un nuevo antiinflamatorio mantiene la eficacia de los glucocorticoides con efectos secundarios reducidos". Endocrinología molecular . 17 (5): 860–9. doi :10.1210/me.2002-0355. PMID 12586843. S2CID 10888190.
- ^ ab Reichardt HM, Kaestner KH, Tuckermann J, Kretz O, Wessely O, Bock R, Gass P, Schmid W, Herrlich P, Angel P, Schütz G (mayo de 1998). "La unión del receptor de glucocorticoides al ADN no es esencial para la supervivencia". Cell . 93 (4): 531–41. doi : 10.1016/S0092-8674(00)81183-6 . PMID 9604929. S2CID 6524157.
- ^ ab Reichardt HM, Tronche F, Bauer A, Schütz G (2000). "Análisis genético molecular de la señalización de glucocorticoides utilizando el sistema Cre/loxP". Química biológica . 381 (9–10): 961–4. doi :10.1515/BC.2000.118. PMID 11076028. S2CID 37837380.
- ^ Schäcke H, Berger M, Rehwinkel H, Asadullah K (septiembre de 2007). "Agonistas selectivos del receptor de glucocorticoides (SEGRA): nuevos ligandos con un índice terapéutico mejorado" (PDF) . Endocrinología molecular y celular . 275 (1–2): 109–17. doi :10.1016/j.mce.2007.05.014. PMID 17630119. S2CID 46020217.
- ^ Cavet ME, Harrington KL, Ward KW, Zhang JZ (2010). "Mapracorat, un nuevo agonista selectivo del receptor de glucocorticoides, inhibe la liberación de citocinas inducida por hiperosmolaridad y las vías MAPK en células epiteliales corneales humanas". Molecular Vision . 16 : 1791–800. PMC 2932489 . PMID 20824100.
- ^ Número de ensayo clínico NCT00944632 para "Aumento de la dosis de diferentes concentraciones de ZK 245186 en dermatitis atópica" en ClinicalTrials.gov
- ^ Número de ensayo clínico NCT01230125 para "Suspensión oftálmica Mapracorat para el tratamiento de la inflamación ocular después de la cirugía de cataratas" en ClinicalTrials.gov
- ^ Stock T, Fleishaker D, Mukherjee A, Le V, Xu J, Zeiher B (2009). "Evaluación de la seguridad, farmacocinética y farmacodinamia de un modulador selectivo del receptor de glucocorticoides (SGRM) en voluntarios sanos". Arthritis Rheum . 60 (Suppl 10): 420. doi :10.1002/art.25503 (inactivo 2024-09-13). Archivado desde el original el 2016-03-03.
{{cite journal}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ) - ^ Hu X, Du S, Tunca C, Braden T, Long KR, Lee J, Webb EG, Dietz JD, Hummert S, Rouw S, Hegde SG, Webber RK, Obukowicz MG (agosto de 2011). "Los antagonistas, pero no los agonistas parciales, de los ligandos del receptor de glucocorticoides muestran una disociación sustancial de los efectos secundarios". Endocrinología . 152 (8): 3123–34. doi : 10.1210/en.2010-1447 . PMID 21558312.
- ^ Número de ensayo clínico NCT01393639 para "Estudio que compara dosis de un compuesto glucocorticoide experimental con prednisona y placebo en la artritis reumatoide" en ClinicalTrials.gov
- ^ Schäcke H, Hennekes H, Schottelius A, Jaroch S, Lehmann M, Schmees N, Rehwinkel H, Asadullah K (2002). "SEGRAs: una nueva clase de compuestos antiinflamatorios". En Cato AC, Schäcke H, Asadullah K (eds.). Avances recientes en la acción del receptor de glucocorticoides . Taller de la Fundación de Investigación Ernst Schering. Vol. 40. Springer. págs. 357–71. doi :10.1007/978-3-662-04660-9_20. ISBN 978-3-662-04662-3. Número de identificación personal 12355726.
- ^ Kerscher MJ, Hart H, Korting HC, Stalleicken D (abril de 1995). "Evaluación in vivo de la potencia atrofogénica del furoato de mometasona, un glucocorticoide tópico potente clorado recientemente desarrollado en comparación con otros glucocorticoides tópicos antiguos y nuevos". Revista internacional de farmacología clínica y terapéutica . 33 (4): 187–9. PMID 7620686.
- ^ Shah S, King EM, Chandrasekhar A, Newton R (mayo de 2014). "Funciones de la fosfatasa de la proteína quinasa activada por mitógeno (MAPK), DUSP1, en el control por retroalimentación de la expresión y represión de genes inflamatorios por dexametasona". The Journal of Biological Chemistry . 289 (19): 13667–79. doi : 10.1074/jbc.M113.540799 . PMC 4036371 . PMID 24692548.
- ^ Ayroldi E, Macchiarulo A, Riccardi C (diciembre de 2014). "Efectos secundarios de los glucocorticoides: modulador selectivo del receptor de glucocorticoides o cremallera de leucina inducida por glucocorticoides? Una perspectiva". Revista FASEB . 28 (12): 5055–70. doi : 10.1096/fj.14-254755 . PMID 25205742. S2CID 40874311.
Lectura adicional
- Hobson, Adrian (2023). La química medicinal de los moduladores del receptor de glucocorticoides . Springer Nature. ISBN 978-3-031-28732-9.