Fotoquímica orgánica
La fotoquímica orgánica abarca las reacciones orgánicas que se inducen por la acción de la luz. [1] [2] La absorción de luz ultravioleta por las moléculas orgánicas a menudo conduce a reacciones. En los primeros tiempos, se utilizaba la luz solar, mientras que en tiempos más modernos se emplean lámparas ultravioleta. La fotoquímica orgánica ha demostrado ser una herramienta sintética muy útil. Se pueden obtener productos orgánicos complejos de forma sencilla.
Historia
Los primeros ejemplos se descubrieron a menudo mediante la observación de precipitados o cambios de color en muestras expuestas a la luz solar. El primer caso informado fue el de Ciamician, que afirmaba que la luz solar convertía la santonina en un fotoproducto amarillo: [3]

Un ejemplo temprano de un precipitado fue la fotodimerización del antraceno , caracterizado por Yulii Fedorovich Fritzsche y confirmado por Elbs. [4] Observaciones similares se centraron en la dimerización del ácido cinámico al ácido truxílico . Ahora se reconocen muchos fotodímeros, por ejemplo, el dímero de pirimidina , el tiofosgeno y el diamantano .
Otro ejemplo fue descubierto por Egbert Havinga en 1956. [5] El curioso resultado fue la activación por fotólisis por un grupo meta nitro en contraste con la activación habitual por los grupos orto y para.

La fotoquímica orgánica avanzó con el desarrollo de las reglas de Woodward-Hoffmann . [6] [7] Estas reglas, que son ilustrativas, ayudan a racionalizar el cierre del anillo electrocíclico impulsado fotoquímicamente del hexa-2,4-dieno, que se produce de manera disrotatoria.
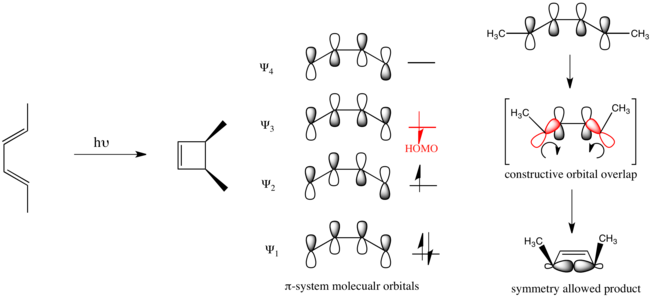
Se dice que las reacciones orgánicas que obedecen a estas reglas tienen simetría permitida. Las reacciones que siguen el curso opuesto tienen simetría prohibida y requieren sustancialmente más energía para llevarse a cabo, si es que se llevan a cabo.
Reacciones clave
Las reacciones fotoquímicas orgánicas se explican en el contexto de los estados excitados relevantes . [8] [9]
Paralelamente a los estudios estructurales descritos anteriormente, se evaluó el papel de la multiplicidad de espín (singlete vs. triplete) en la reactividad. Se destacó la importancia de las especies excitadas por tripletes. Los tripletes tienden a tener una vida más larga que los singletes y una energía menor que el singlete de la misma configuración. Los tripletes pueden surgir de (A) la conversión de los singletes formados inicialmente o por (B) la interacción con un triplete de mayor energía (sensibilización).
Es posible extinguir las reacciones triplete. [10]
Las reacciones fotoquímicas orgánicas comunes incluyen: Norrish Tipo I , Norrish Tipo II , la racemización de bifenilos ópticamente activos, el reordenamiento de ciclohexadienona tipo A, el reordenamiento de ciclohexenona tipo B, el reordenamiento de di- π -metano , el reordenamiento de biciclo[3.1.0]hexanona tipo B a fenoles, procesos electrocíclicos fotoquímicos , el reordenamiento de epoxicetonas a beta-dicetonas, la apertura de anillo de ciclopropilcetonas, la heterolisis de derivados 3,5-dimetoxilbencílicos y las ciclizaciones fotoquímicas de dienos.
Consideraciones prácticas

Los reactivos de las fotorreacciones pueden ser tanto gaseosos como líquidos. [11] En general, es necesario acercar los reactivos a la fuente de luz para obtener la mayor eficacia luminosa posible . Para ello, la mezcla de reacción puede irradiarse directamente o en un brazo lateral de flujo continuo de un reactor con una fuente de luz adecuada. [12]
Una desventaja de los procesos fotoquímicos es la baja eficiencia de la conversión de energía eléctrica en energía de radiación de la longitud de onda requerida . Además de la radiación, las fuentes de luz generan mucho calor, lo que a su vez requiere energía de refrigeración. Además, la mayoría de las fuentes de luz emiten luz policromática, aunque solo se necesita luz monocromática . [13] Sin embargo, un alto rendimiento cuántico compensa estas desventajas.
Trabajar a bajas temperaturas es ventajoso ya que se evitan reacciones secundarias (ya que aumenta la selectividad) y se incrementa el rendimiento (ya que los reactivos gaseosos se expulsan menos del disolvente).
Los materiales de partida pueden enfriarse antes de la reacción hasta el punto de que el calor de reacción se absorba sin enfriar más la mezcla. En el caso de materiales de partida gaseosos o de bajo punto de ebullición, es necesario trabajar bajo sobrepresión. Debido a la gran cantidad de posibles materias primas, se han descrito una gran cantidad de procesos. [14] [15] Las reacciones a gran escala generalmente se llevan a cabo en un reactor de tanque agitado , un reactor de columna de burbujeo o un reactor de tubo, seguido de un procesamiento adicional según el producto objetivo. [16] En el caso de un reactor de tanque agitado, la lámpara (generalmente con forma de cilindro alargado) está provista de una camisa de enfriamiento y se coloca en la solución de reacción. Los reactores de tubo están hechos de tubos de cuarzo o vidrio, que se irradian desde el exterior. El uso de un reactor de tanque agitado tiene la ventaja de que no se pierde luz al medio ambiente. Sin embargo, la intensidad de la luz disminuye rápidamente con la distancia a la fuente de luz debido a la adsorción por los reactivos. [12]
La influencia de la radiación sobre la velocidad de reacción se puede representar a menudo mediante una ley de potencia basada en la densidad de flujo cuántico, es decir, el cuanto de luz molar (anteriormente medido en la unidad einstein ) por área y tiempo. Por lo tanto, un objetivo en el diseño de reactores es determinar el dimensionamiento económicamente más favorable con respecto a una optimización de la densidad de corriente cuántica. [17]
Estudios de caso
[2+2] Cicloadiciones
Las olefinas se dimerizan con la irradiación UV. [18]
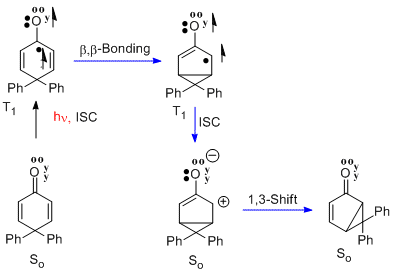
Reordenamiento de 4,4-difenilciclohexadienona
Un ejemplo muy similar al de la santonina a la lumisantonina es el reordenamiento de la 4,4-difenilciclohexadienona [9]. En este caso, el estado excitado del triplete n-pi* sufre el mismo enlace beta-beta. A esto le sigue un cruce entre sistemas (es decir, ISC) para formar el estado fundamental singlete, que se ve como un zwitterión . El paso final es el reordenamiento al fotoproducto bicíclico. La reacción se denomina reordenamiento de ciclohexadienona tipo A.
4,4-difenilciclohexenona
Para proporcionar más evidencia sobre el mecanismo de la dienona en el que hay unión entre los dos enlaces dobles, se presenta aquí el caso de la 4,4-difenilciclohexenona. Se observa que la reorganización es bastante diferente; por lo tanto, se requieren dos enlaces dobles para una reorganización de tipo A. Con un enlace doble, uno de los grupos fenilo, originalmente en C-4, ha migrado a C-3 (es decir, el carbono beta). [19]
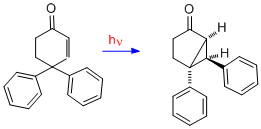
Cuando uno de los grupos arilo tiene un grupo para-ciano o para-metoxi, ese grupo arilo sustituido migra con preferencia. [20] La inspección de las especies alternativas de tipo fenonio, en las que un grupo arilo ha comenzado a migrar al carbono beta, revela una mayor deslocalización electrónica con un sustituyente para en el grupo arilo que migra y, por lo tanto, una vía más estabilizada.

π-π* reactividad
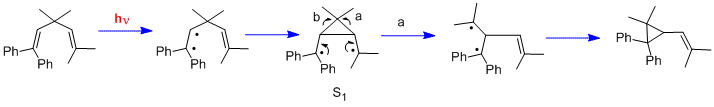
Otro tipo de reacción fotoquímica es el reordenamiento del di- π -metano . [21] Otros dos ejemplos tempranos fueron el reordenamiento del 1,1,5,5-tetrafenil-3,3-dimetil-1,4-pentadieno (la molécula "Mariano") [22] y el reordenamiento del barreleno a semibullvaleno . [23] Observamos que, en contraste con las reacciones de ciclohexadienona que usaban estados excitados n- π *, los reordenamientos del di- π -metano utilizan estados excitados π - π *.
Temas relacionados
Catálisis foto-redox
En la catálisis fotorredox , el fotón es absorbido por un sensibilizador (molécula de antena o ion) que luego efectúa reacciones redox en el sustrato orgánico. Un sensibilizador común es la tris(bipiridina) de rutenio(II) . Algunas reacciones de aminotrifluorometilación son ilustrativas de la catálisis fotorredox. [24]

Fotocloración
La fotocloración es una de las mayores aplicaciones de la fotoquímica a la síntesis orgánica. Sin embargo, el fotón no es absorbido por el compuesto orgánico, sino por el cloro . La fotólisis del Cl2 produce átomos de cloro, que extraen átomos de H de los hidrocarburos, lo que da lugar a la cloración.
Referencias
- ^ P. Klán, J. Wirz Fotoquímica de compuestos orgánicos: de los conceptos a la práctica. Wiley, Chichester, 2009, ISBN 978-1405190886 .
- ^ NJ Turro, V. Ramamurthy, JC Scaiano Fotoquímica molecular moderna de moléculas orgánicas. University Science Books, Sausalito, 2010, ISBN 978-1891389252 .
- ^ Roth, Heinz D. (1989). "Los inicios de la fotoquímica orgánica". Angewandte Chemie International Edition en inglés . 28 (9): 1193–1207. doi :10.1002/anie.198911931.
- ^ Elbs, Karl (30 de junio de 1891). "Ueber Parantraceno". Revista para la química práctica . 44 (1): 467–469. doi :10.1002/prac.18910440140. ISSN 0021-8383.
- ^ Tenera, E.; De Jongh, RO; Dorst, W. (1956). "Aceleración fotoquímica de la hidrólisis de fosfatos de nitrofenilo y sulfatos de nitrofenilo". Recueil des Travaux Chimiques des Pays-Bas . 75 (4): 378–383. doi :10.1002/recl.19560750403.
- ^ Woodward, RB; Hoffmann, Roald (1969). "La conservación de la simetría orbital". Angew. Chem. Int. Ed . 8 (11): 781–853. doi :10.1002/anie.196907811.
- ^ Woodward, RB; Hoffmann, Roald (1971). La conservación de la simetría orbital (3.ª edición, 1.ª edición). Weinheim, BRD: Verlag Chemie GmbH (BRD) y Academic Press (EE. UU.). pp. 1–178. ISBN 978-1483256153.
- ^ "El reordenamiento fotoquímico de la 4,4-difenilciclohexadienona. Documento I sobre una teoría general de las reacciones fotoquímicas", Zimmerman, HE; Schuster, DIJ Am. Chem. Soc., 1961, 83, 4486–4487.
- ^ ab Zimmerman, Howard E.; David I. Schuster (1962). "Un nuevo enfoque de la fotoquímica orgánica mecanicista. IV. Reordenamientos fotoquímicos de la 4,4-difenilciclohexadienona". Revista de la Sociedad Química Americana . 84 (23). ACS: 4527–4540. doi :10.1021/ja00882a032.
- ^ "Terenin, A.; Ermolaev, V. Fosforescencia sensibilizada en soluciones orgánicas a baja temperatura; transferencia de energía entre estados tripletes", Trans. Faraday Soc., 1956, 52, 1042–1052.
- ^ Mario Schiavello (Ed.): Fotoelectroquímica, fotocatálisis y fotorreactores: fundamentos y desarrollos . Springer Países Bajos, 2009, ISBN 978-90-481-8414-9 , pág. 564.
- ^ de Martin Fischer: Aplicaciones industriales de las síntesis fotoquímicas. En: Angewandte Chemie International, edición en inglés. 17, 1978, págs. 16-26, doi:10.1002/anie.197800161.
- ^ Dieter Wöhrle, Michael W. Tausch, Wolf-Dieter Stohrer: Fotoquímica: Konzepte, Methoden, Experimente . Wiley & Sons, 1998, ISBN 978-3-527-29545-6 , págs.
- ^ Subvención estadounidense 1379367, F. Sparre y WE Masland, "Proceso de cloración", expedida el 24 de mayo de 1921, asignada a Du Pont
- ^ Subvención estadounidense 1459777, R. Leiser & F. Ziffer, "Proceso y aparato para la cloración de metano", expedida el 14 de febrero de 1920, asignada a Ziffer Fritz y Leiser Richard
- ^ David A. Mixon, Michael P. Bohrer, Patricia A. O'Hara: Ultrapurificación de SiCl4 mediante fotocloración en un reactor de columna de burbujas. En: AIChE Journal. 36, 1990, págs. 216–226, doi:10.1002/aic.690360207.
- ^ H. Hartig: Einfache Dimensionierung, photochemischer Reaktoren . En: Chemie Ingenieur Technik – CIT . 42, 1970, págs. 1241–1245, doi :10.1002/cite.330422002.
- ^ Cargill1, RL; Dalton, JR; Morton, GH; Caldwell1, WE (1984). "Fotociclización de una enona a un alqueno: 6-metilbiciclo[4.2.0]octan-2-ona". Organic Syntheses . 62 : 118. doi :10.15227/orgsyn.062.0118.
{{cite journal}}: CS1 maint: nombres numéricos: lista de autores ( enlace ) - ^ "Fotoquímica orgánica mecanicista y exploratoria, IX. Migración de fenilo en la irradiación de 4,4-difenilciclohexenona", Zimmerman, HE; Wilson, JWJ Am. Chem. Soc., 1964, 86, 4036–4042.
- ^ "Aptitud fotoquímica migratoria en ciclohexenonas. Fotoquímica orgánica mecanicista y exploratoria. XXIII", Zimmerman, HE; Scheffer, JRJ Am. Chem. Soc., 1967, 89, 2033–2047.
- ^ "Sustitución asimétrica y dirección del reordenamiento del di-pi-metano; fotoquímica orgánica mecanicista y exploratoria. LVI", Zimmerman, HE; Pratt, ACJ Am. Chem. Soc., 1970, 92, 6259–6267
- ^ "El reordenamiento del di-pi-metano. Interacción de cromóforos vinílicos excitados electrónicamente. Zimmerman, HE; Mariano, PSJ Am. Chem. Soc., 1969, 91, 1718–1727.
- ^ Zimmerman, HE; Grunewald, GL (1966). "La química del barreleno. III. Una fotoisomerización única del semibullvaleno". J. Am. Chem. Soc. 88 (1): 183–184. doi :10.1021/ja009
- ^ Yasu, Yusuke; Koike, Takashi; Akita, Munetaka (17 de septiembre de 2012). "Oxitrifluorometilación de tres componentes de alquenos: difuncionalización altamente eficiente y regioselectiva de enlaces C=C mediada por catalizadores fotorredox". Angewandte Chemie International Edition . 51 (38): 9567–9571. doi :10.1002/anie.201205071. PMID 22936394.