Tungstato
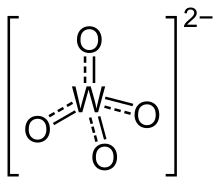
En química , un tungstato es un compuesto que contiene un oxianión de tungsteno o es un óxido mixto que contiene tungsteno. El ion de tungstato más simple es WO2−4, "ortotungstato". [1] Muchos otros tungstatos pertenecen a un gran grupo de iones poliatómicos que se denominan polioxometalatos ("POM"), y específicamente se denominan isopolioxometalatos, ya que contienen, junto con oxígeno y tal vez hidrógeno, solo otro elemento. Casi todos los minerales de tungsteno útiles son tungstatos. [2]
Estructuras
Los ortotungstatos presentan centros tetraédricos W(VI) con distancias W–O cortas de 1,79 Å . Estructuralmente, se parecen a los sulfatos. El tungsteno octaédrico de seis coordenadas predomina en los polioxotungstatos. En estos compuestos, las distancias W–O son alargadas. [1]
Algunos ejemplos de iones de tungstato: [3]
- HWO−4(hidrogenoungstato) [3]
- W2O polimérico2−7iones de diversas estructuras en Na 2 W 2 O 7 , Li 2 W 2 O 7 y Ag 2 W 2 O 7 [4]
- [W 7 O 24 ] 6− (paratungstato A) [3]
- [W 10 O 32 ] 4− (tungstato Y) [5]
- [H 2 W 12 O 42 ] 10− (paratungstato B) [3]
- α-[H 2 W 12 O 40 ] 6− (metacungstato) [5]
- β-[H 2 W 12 O 40 ] 6− (tungstato X) [5]
Consulte la categoría de tungstatos para obtener una lista de tungstatos.
Aparición
Los tungstatos se encuentran de forma natural junto con los molibdatos . La scheelita , el mineral de tungstato de calcio, a menudo contiene una pequeña cantidad de molibdato. La wolframita es tungstato de manganeso y hierro, y todos ellos son fuentes valiosas de tungsteno. La powellita es una forma mineral de molibdato de calcio que contiene una pequeña cantidad de tungstato.
Reacciones
Las soluciones de tungstatos, como las de molibdatos , dan soluciones intensamente azules de tungstato (V, VI) complejo análogo a los azules del molibdeno cuando se reducen con la mayoría de los materiales orgánicos. [1]
A diferencia del cromato , el tungstato no es un buen oxidante , pero al igual que el cromato, las soluciones de tungstato se condensan para dar isopolitungstatos tras la acidificación.
Referencias
- ^ abc Egon Wiberg, Arnold Frederick Holleman (2001). Química inorgánica . Elsevier. ISBN 0-12-352651-5.
- ^ Lassner, Erik; Schubert, Wolf-Dieter; Lüderitz, Eberhard; Lobo, Hans Uwe (2005). "Tungsteno, aleaciones de tungsteno y compuestos de tungsteno". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a27_229. ISBN 978-3527306732.
- ^ abcd Greenwood, Norman N. ; Earnshaw, Alan (1997). Química de los elementos (2.ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ Wells AF (1984) Química inorgánica estructural, quinta edición, Oxford Science Publications, ISBN 0-19-855370-6
- ^ abc Jon A. McCleverty, NG Connelly, Nomenclatura de la química inorgánica II: recomendaciones 2000, Comisión de Nomenclatura de la Química Inorgánica de la Unión Internacional de Química Pura y Aplicada, publicado por la Royal Society of Chemistry, 2001, ISBN 0-85404-487-6