Reacción de Maillard

La reacción de Maillard ( / m aɪ ˈ j ɑːr / my- YAR ; francés: [majaʁ] ) es una reacción química entre aminoácidos y azúcares reductores para crear melanoidinas , los compuestos que dan a los alimentos dorados su sabor distintivo. Los filetes chamuscados , las albóndigas fritas, las galletas y otros tipos de bizcochos, los panes, los malvaviscos tostados, el falafel y muchos otros alimentos experimentan esta reacción. Lleva el nombre del químico francés Louis Camille Maillard , quien la describió por primera vez en 1912 mientras intentaba reproducir la síntesis biológica de proteínas . [1] [2] La reacción es una forma de pardeamiento no enzimático que normalmente se produce rápidamente de alrededor de 140 a 165 °C (280 a 330 °F). Muchas recetas requieren una temperatura del horno lo suficientemente alta como para garantizar que se produzca una reacción de Maillard. [3] A temperaturas más altas, la caramelización (el oscurecimiento de los azúcares, un proceso distinto) y posteriormente la pirólisis (la descomposición final que conduce a la quema y al desarrollo de sabores acres) se vuelven más pronunciadas. [4]
El grupo carbonilo reactivo del azúcar reacciona con el grupo amino nucleofílico del aminoácido y forma una mezcla compleja de moléculas poco caracterizadas responsables de una variedad de aromas y sabores. Este proceso se acelera en un entorno alcalino (por ejemplo, lejía aplicada para oscurecer pretzels; ver panecillo con lejía ), ya que los grupos amino ( RNH+3→ RNH 2 ) se desprotonan y, por lo tanto, tienen una nucleofilia aumentada . Esta reacción es la base de muchas de las recetas de la industria de los aromas . A altas temperaturas, se puede formar un probable carcinógeno llamado acrilamida [5] . [6] Esto se puede evitar calentando a una temperatura más baja, añadiendo asparaginasa o inyectando dióxido de carbono. [5]
En el proceso de cocción, las reacciones de Maillard pueden producir cientos de compuestos de sabor diferentes según los componentes químicos de los alimentos, la temperatura, el tiempo de cocción y la presencia de aire. Estos compuestos, a su vez, suelen descomponerse para formar aún más compuestos de sabor. Los científicos especializados en sabores han utilizado la reacción de Maillard a lo largo de los años para crear sabores artificiales; la mayoría de las patentes están relacionadas con la producción de sabores similares a los de la carne. [7]
Historia
En 1912, Louis Camille Maillard publicó un artículo que describía la reacción entre aminoácidos y azúcares a temperaturas elevadas. [1] En 1953, el químico John E. Hodge, del Departamento de Agricultura de los Estados Unidos , estableció un mecanismo para la reacción de Maillard. [8] [9]
Alimentos y productos

La reacción de Maillard es responsable de muchos colores y sabores en los alimentos, como el dorado de varias carnes cuando se dora o se asa a la parrilla, el dorado y el sabor umami de las cebollas fritas y el café tostado . Contribuye a la corteza oscura de los productos horneados , el color marrón dorado de las papas fritas y otras patatas fritas, el dorado de la cebada malteada que se encuentra en el whisky de malta y la cerveza, y el color y el sabor de la leche en polvo y condensada , el dulce de leche , el toffee , el ajo negro , el chocolate , los malvaviscos tostados y los cacahuetes tostados . [ cita requerida ]
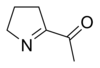
La 6-acetil-2,3,4,5-tetrahidropiridina es responsable del sabor a galleta o a galleta salada presente en productos horneados como pan, palomitas de maíz y productos de tortilla. El compuesto estructuralmente relacionado 2-acetil-1-pirrolina tiene un olor similar y también se produce de forma natural sin calentar. El compuesto le da a las variedades de arroz cocido y a la hierba pandan ( Pandanus amaryllifolius ) sus olores típicos. Ambos compuestos tienen umbrales de olor por debajo de 0,06 nanogramos por litro. [10]


Las reacciones de oscurecimiento que ocurren cuando la carne se asa o se dora son complejas y ocurren principalmente por oscurecimiento de Maillard [11] con contribuciones de otras reacciones químicas, incluida la descomposición de los anillos de tetrapirrol de la proteína muscular mioglobina . Las reacciones de Maillard también ocurren en la fruta seca [12] y cuando el champán envejece en la botella [13].
La caramelización es un proceso completamente diferente del oscurecimiento por reacción de Maillard, aunque los resultados de ambos procesos a veces son similares a simple vista (y a las papilas gustativas). La caramelización a veces puede causar oscurecimiento en los mismos alimentos en los que se produce la reacción de Maillard, pero los dos procesos son distintos. Ambos se promueven mediante el calor, pero la reacción de Maillard implica aminoácidos, mientras que la caramelización es la pirólisis de ciertos azúcares. [14]
Al hacer ensilaje , el exceso de calor provoca la reacción de Maillard, que reduce la cantidad de energía y proteínas disponibles para los animales que se alimentan de él. [15]
Arqueología
En arqueología, el proceso de Maillard ocurre cuando los cuerpos se conservan en turberas . El ambiente ácido de la turba provoca un bronceado o amarronamiento de los tonos de la piel y puede hacer que el cabello adquiera un tono rojizo o rojizo. El mecanismo químico es el mismo que el del amarronamiento de los alimentos, pero se desarrolla lentamente con el tiempo debido a la acción ácida sobre el cuerpo de la turbera . Se observa típicamente en cuerpos de la Edad del Hierro y fue descrito por Painter en 1991 como la interacción del ácido anaeróbico, ácido y frío (normalmente 4 °C (39 °F)) del esfagno sobre los polisacáridos .
La reacción de Maillard también contribuye a la preservación de las paleoheces . [16]
Mecanismo químico
- El grupo carbonilo del azúcar reacciona con el grupo amino del aminoácido, produciendo glicosilamina N-sustituida y agua.
- La glicosilamina inestable sufre un reordenamiento de Amadori , formando cetosaminas.
- Se conocen varias formas en las que las cetosaminas pueden reaccionar posteriormente:
- Produce dos moléculas de agua y reductonas.
- Se pueden formar diacetilo , piruvaldehído y otros productos de fisión hidrolítica de cadena corta.
- Produce polímeros nitrogenados marrones y melanoidinas.
Los productos Amadori de cadena abierta experimentan una mayor deshidratación y desaminación para producir dicarbonilos. [17] Este es un intermedio crucial.
Los dicarbonilos reaccionan con aminas para producir aldehídos de Strecker a través de la degradación de Strecker . [18]
La acrilamida , un posible carcinógeno humano , [19] puede generarse como un subproducto de la reacción de Maillard entre azúcares reductores y aminoácidos, especialmente asparagina , ambos presentes en la mayoría de los productos alimenticios. [20] [21]
Véase también
Referencias
- ^ ab Maillard, LC (1912). "Action des acides amines sur les sucres;formation de melanoidines par voie méthodique" [Acción de los aminoácidos sobre los azúcares. Formación de melanoidinas de forma metódica. Comptes Rendus (en francés). 154 : 66–68.
- ^ Chichester, CO, ed. (1986). Avances en la investigación alimentaria . Avances en la investigación sobre alimentación y nutrición. Vol. 30. Boston: Academic Press. pág. 79. ISBN 0-12-016430-2.
- ^ Bui, Andrew (29 de septiembre de 2017). "Por qué tantas recetas requieren un horno a 350 grados". Mesa de degustación . Consultado el 6 de noviembre de 2017 .
- ^ "Aquí se explica cómo dorar un filete a la perfección". Home Cook World . 2021-09-06. Archivado desde el original el 2022-01-27 . Consultado el 2022-01-27 .
- ^ ab Tamanna, N; Mahmood, N (2015). "Procesamiento de alimentos y productos de la reacción de Maillard: efecto sobre la salud y la nutrición humanas". Revista internacional de ciencia de los alimentos . 2015 : 526762. doi : 10.1155/2015/526762 . ISSN 2314-5765. PMC 4745522. PMID 26904661 .
- ^ ab Tareke, E.; Rydberg, P.; Karlsson, Patrik; Eriksson, Sune; Törnqvist, Margareta (2002). "Análisis de acrilamida, carcinógeno formado en alimentos calentados". J. Agrícola. Química de los alimentos . 50 (17): 4998–5006. doi :10.1021/jf020302f. PMID 12166997.
- ^ Danehy, James P. (19 de mayo de 1986). Chicester, CO (ed.). "Reacciones de Maillard: pardeamiento no enzimático en sistemas alimentarios con especial referencia al desarrollo del sabor" (PDF) . Avances en la investigación alimentaria . 30. Academic Press: 107. PMID 3526830. Consultado el 15 de marzo de 2024 .
- ^ Hodge, JE (1953). "Alimentos deshidratados, química de las reacciones de pardeamiento en sistemas modelo". Revista de química agrícola y alimentaria . 1 (15): 928–43. doi :10.1021/jf60015a004.
- ^ Everts, Sarah (1 de octubre de 2012). "La reacción de Maillard cumple 100 años". Chemical & Engineering News . 90 (40): 58–60. doi :10.1021/cen-09040-scitech2.
- ^ Harrison, TJ; v, GR (2005). "Una construcción rápida y de alto rendimiento de los compuestos aromáticos alimentarios 6-acetil-1,2,3,4-tetrahidropiridina y 2-acetil-1-pirrolina". J. Org. Chem. 70 (26): 10872–74. doi :10.1021/jo051940a. PMID 16356012.
- ^ McGee, Harold (2004). Sobre la comida y la cocina: la ciencia y la tradición de la cocina . Nueva York: Scribner. pp. 778–79. ISBN 978-0-684-80001-1.
- ^ Miranda, Gonzalo; Berna, Angel; Mulet, Antonio (4 de febrero de 2019). "Almacenamiento de frutos secos: un análisis de los cambios atmosféricos en el espacio de cabeza del envase". Alimentos . 8 (2): 56. doi : 10.3390/foods8020056 . PMC 6406843 . PMID 30720722.
- ^ Liem, Peter (2017). Champagne: La guía esencial de los vinos, productores y terroirs de la emblemática región . Ten Speed Press. pág. 66. ISBN 978-1784724474.
- ^ Krystal, Becky (31 de enero de 2020). «La reacción de Maillard: qué es y por qué es importante». The Washington Post . Consultado el 28 de julio de 2022 .
- ^ Cooper, Phil (2 de mayo de 2017). "Estabilidad del ensilaje de pasto y ensilaje de Maillard". Farm Consultancy . Consultado el 2 de agosto de 2022 .
- ^ Dove, Alan (11 de febrero de 2016). «Secuenciación de núcleo duro». Science . Asociación Estadounidense para el Avance de la Ciencia . Consultado el 16 de junio de 2021 .
En un ambiente seco, la reacción de Maillard (el mismo proceso químico que dora un filete) hace que las heces desarrollen una capa exterior protectora.
- ^ Nursten, Harry (2007). "La química del pardeamiento no enzimático". La reacción de Maillard . págs. 5–30. doi :10.1039/9781847552570-00005. ISBN 978-0-85404-964-6.
- ^ Stadler, Richard H.; Robert, Fabien; Riediker, Sonja; Varga, Natalia; Davidek, Tomas; Devaud, Stéphanie; Goldmann, Till; Hau, Jörg; Blank, Imre (agosto de 2004). "Estudio mecanicista en profundidad sobre la formación de acrilamida y otros compuestos vinílicos mediante la reacción de Maillard". Revista de química agrícola y alimentaria . 52 (17): 5550–5558. doi :10.1021/jf0495486. PMID 15315399.
- ^ Acrilamida. Cancer.org. Consultado el 24 de julio de 2016.
- ^ Virk-Baker, Mandeep K.; Nagy, Tim R.; Barnes, Stephen; Groopman, John (29 de mayo de 2014). "Acrilamida dietética y cáncer humano: una revisión sistemática de la literatura". Nutrición y cáncer . 66 (5): 774–790. doi :10.1080/01635581.2014.916323. PMC 4164905 . PMID 24875401.
- ^ Mottram, Donald S.; Wedzicha, Bronislaw L.; Dodson, Andrew T. (octubre de 2002). "La acrilamida se forma en la reacción de Maillard". Nature . 419 (6906): 448–449. Bibcode :2002Natur.419..448M. doi :10.1038/419448a. PMID 12368844. S2CID 4360610.
Lectura adicional
- Van Soest, Peter J. (1982). Ecología nutricional del rumiante (2ª ed.). Ithaca, Nueva York: Cornell University Press. ISBN 9780801427725 . OCLC 29909839.




