Espectroscopia de resonancia magnética nuclear de flúor-19

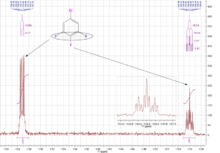
La espectroscopia de resonancia magnética nuclear de flúor-19 ( RMN de flúor o RMN 19 F ) es una técnica analítica utilizada para detectar e identificar compuestos que contienen flúor. El 19 F es un núcleo importante para la espectroscopia de RMN debido a su receptividad y gran dispersión de desplazamiento químico , que es mayor que la de la espectroscopia de resonancia magnética nuclear de protones . [1] [2] [3]
Detalles operativos
El 19 F tiene un espín nuclear (I) de 1 ⁄ 2 y una alta relación giromagnética . En consecuencia, este isótopo es muy sensible a las mediciones de RMN. Además, el 19 F comprende el 100 % del flúor natural. El único otro espín altamente sensible1/2Los núcleos activos de RMN que son monoisotópicos (o casi) son 1 H y 31 P. [4] [a] De hecho, el núcleo 19 F es el tercer núcleo de RMN más receptivo, después del núcleo 3 H y el núcleo 1 H.
Los desplazamientos químicos de RMN de 19 F abarcan un rango de aproximadamente 800 ppm. Para los compuestos organofluorados , el rango es más estrecho, de aproximadamente -50 a -70 ppm (para los grupos CF3 ) a -200 a -220 ppm (para los grupos CH2F ) . El rango espectral tan amplio puede causar problemas en el registro de espectros, como una resolución de datos deficiente y una integración imprecisa.
También es posible registrar espectros desacoplados de 19 F{ 1 H} y 1 H{ 19 F} y correlaciones de enlaces múltiples 19 F- 13 C HMBC y espectros HOESY a través del espacio.
Desplazamientos químicos
Los desplazamientos químicos de RMN de 19 F en la literatura varían considerablemente, comúnmente en más de 1 ppm, incluso dentro del mismo disolvente. [5] Aunque el compuesto de referencia para la espectroscopia de RMN de 19 F, CFCl 3 puro (0 ppm), [6] se ha utilizado desde la década de 1950, [7] hasta hace poco no existían instrucciones claras sobre cómo medirlo y utilizarlo en mediciones de rutina. [5] Una investigación de los factores que influyen en el desplazamiento químico en la espectroscopia de RMN de flúor reveló que el disolvente tenía el mayor efecto (Δδ = ±2 ppm o más). [5] Se ha preparado una tabla de referencia específica del disolvente con 5 compuestos de referencia internos ( CFCl 3 , C 6 H 5 F , PhCF 3 , C 6 F 6 y CF 3 CO 2 H ) para permitir una referencia reproducible con una precisión de Δδ = ±30 ppb. [5] Como el desplazamiento químico del CFCl 3 también se ve afectado por el solvente, se debe tener cuidado al utilizar CFCl 3 disuelto como compuesto de referencia con respecto al desplazamiento químico del CFCl 3 puro (0 ppm). [5] Ejemplo de desplazamientos químicos determinados frente al CFCl 3 puro : [5]
| CFC3 | C6H5F | Fcp 3 | C 6 F 6 | CF3CO2H | |
|---|---|---|---|---|---|
| Solvente | [ppm] | [ppm] | [ppm] | [ppm] | [ppm] |
| CDCl3 | 0,65 | -112,96 | -62,61 | −161,64 | −75,39 |
| CD2Cl2 | 0,02 | −113,78 | −62,93 | −162,61 | −75,76 |
| C 6 Re 6 | -0,19 | -113,11 | -62,74 | −163,16 | −75,87 |
| Acetona - d 6 | -1,09 | −114,72 | -63,22 | −164,67 | −76,87 |
Para obtener una lista completa de los cambios químicos de los compuestos de referencia en 11 disolventes deuterados, se remite al lector a la literatura citada. [5]
También se ha proporcionado recientemente una lista concisa de desplazamientos químicos adecuadamente referenciados de más de 240 sustancias químicas fluoradas. [5]
Predicción del desplazamiento químico
Los desplazamientos químicos de RMN de 19 F son más difíciles de predecir que los de RMN de 1 H. En concreto, los desplazamientos de RMN de 19 F se ven fuertemente afectados por las contribuciones de los estados electrónicos excitados, mientras que los desplazamientos de RMN de 1 H están dominados por las contribuciones diamagnéticas. [8]
Compuestos de fluorometilo
| -R | δ (ppm) |
|---|---|
| yo | −78 |
| Capítulo 3 | -62 |
| Canal 2 Canal 3 | -70 |
| CH2NH2 | -72 |
| CH2OH | −78 |
| CH= CH2 | −67 |
| C≡CH | −56 |
| CF3 | -89 |
| CF2CF3 | −83 |
| F | −63 |
| Cl | −29 |
| Es | -18 |
| I | -5 |
| OH | -55 |
| NH2 | −49 |
| EL | -32 |
| C(=O)Ph | −58 |
| C(=O) CF3 | -85 |
| C(=O)OH | −77 |
| C(=O)F | −76 |
| C(= O ) OCH2CH3 | −74 |
| -R | δ (ppm) |
|---|---|
| yo | −144 |
| Capítulo 3 | -110 |
| Canal 2 Canal 3 | -120 |
| CF3 | −141 |
| CF2CF3 | −138 |
| C(=O)OH | −127 |
| -R | δ (ppm) |
|---|---|
| yo | −268 |
| Capítulo 3 | −212 |
| Canal 2 Canal 3 | −212 |
| CH2OH | −226 |
| CF3 | −241 |
| CF2CF3 | −243 |
| C(=O)OH | −229 |
Fluoroalquenos
Para los sustituyentes de flúor vinílico, la siguiente fórmula permite estimar los desplazamientos químicos de 19 F: donde Z es el desplazamiento químico estadístico del sustituyente (SSCS) para el sustituyente en la posición indicada y S es el factor de interacción. [9] Algunos valores representativos para usar en esta ecuación se proporcionan en la siguiente tabla: [10]
| Sustituyente R | Z cis | Z trans | Gema Z |
|---|---|---|---|
| -H | -7,4 | -31,3 | 49,9 |
| -CH3 | -6.0 | −43,0 | 9.5 |
| -CH= CH2 | — | — | 47,7 |
| -Ph | -15,7 | -35,1 | 38.7 |
| -CF3 | -25,3 | −40,7 | 54.3 |
| -F | 0 | 0 | 0 |
| -Cl | -16,5 | -29,4 | — |
| -Br | -17,7 | −40,0 | — |
| -yo | -21,3 | −46,3 | 17.4 |
| -OCH2CH3 | −77,5 | — | 84.2 |
| Sustituyente | Sustituyente | S cis/trans | S cis/gema | S trans/gema |
|---|---|---|---|---|
| -H | -H | -26,6 | — | 2.8 |
| -H | -CF3 | -21,3 | — | — |
| -H | -CH3 | — | 11.4 | — |
| -H | -OCH2CH3 | −47,0 | — | — |
| -H | -Ph | -4,8 | — | 5.2 |
| -CF3 | -H | -7,5 | -10,6 | 12.5 |
| -CF3 | -CF3 | -5,9 | -5,3 | -4,7 |
| -CF3 | -CH3 | 17.0 | — | — |
| -CF3 | -Ph | -15,6 | — | -23,4 |
| -CH3 | -H | — | -12,2 | — |
| -CH3 | -CF3 | — | -13,8 | -8,9 |
| -CH3 | -Ph | — | -19,5 | -19,5 |
| -OCH2CH3 | -H | -5,1 | — | — |
| -Ph | -H | — | — | 20.1 |
| -Ph | -CF3 | -23,2 | — | — |
Fluorobencenos
Para determinar los desplazamientos químicos de 19 F de los átomos de flúor aromático, específicamente los fluoruros de fenilo, existe otra ecuación que permite una aproximación. Adoptada de "Structure Determination of Organic Compounds", [10] esta ecuación es donde Z es el valor SSCS para un sustituyente en una posición dada en relación con el átomo de flúor. Algunos valores representativos para usar en esta ecuación se proporcionan en la siguiente tabla: [10]
| Sustituyente | Orto Z | Z meta | Z para |
|---|---|---|---|
| -CH3 | -3,9 | -0,4 | -3,6 |
| -CH= CH2 | -4,4 | 0,7 | -0,6 |
| -F | -23,2 | 2.0 | -6,6 |
| -Cl | -0,3 | 3.5 | -0,7 |
| -Br | 7.6 | 3.5 | 0,1 |
| -yo | 19.9 | 3.6 | 1.4 |
| -OH | -23,5 | 0 | -13,3 |
| -OCH3 | -18,9 | -0,8 | -9.0 |
| -NH2 | -22,9 | -1,3 | -17,4 |
| -NO 2 | -5,6 | 3.8 | 9.6 |
| -CN | 6.9 | 4.1 | 10.1 |
| -Sh | 10.0 | 0.9 | -3,5 |
| −CH(=O) | -7,4 | 2.1 | 10.3 |
| −C(=O) CH3 | 2.5 | 1.8 | 7.6 |
| -C(=O)OH | 2.3 | 1.1 | 6.5 |
| -C(=O) NH2 | 0,5 | -0,8 | 3.4 |
| −C(=O) OCH3 | 3.3 | 3.8 | 7.1 |
| −C(=O)Cl | 3.4 | 3.5 | 12.9 |
Los datos que se muestran arriba son solo representativos de algunas tendencias y moléculas. Se pueden consultar otras fuentes y tablas de datos para obtener una lista más completa de las tendencias en los desplazamientos químicos del 19 F. Algo que se debe tener en cuenta es que, históricamente, la mayoría de las fuentes bibliográficas cambiaron la convención de usar números negativos. Por lo tanto, tenga cuidado con el signo de los valores informados en otras fuentes. [8]
Acoplamiento espín-espín
Las constantes de acoplamiento de 19 F- 19 F son generalmente mayores que las constantes de acoplamiento de 1 H- 1 H. Se observan comúnmente acoplamientos de largo alcance de 19 F- 19 F ( 2 J, 3 J, 4 J o incluso 5 J). Generalmente, cuanto mayor sea el alcance del acoplamiento, menor será el valor. [11] El hidrógeno se acopla con el flúor, lo que es muy típico de ver en el espectro de 19 F. Con un hidrógeno geminal, las constantes de acoplamiento pueden ser tan grandes como 50 Hz. Otros núcleos pueden acoplarse con flúor, sin embargo, esto se puede evitar realizando experimentos desacoplados. Es común realizar RMN de flúor con carbono y protón desacoplados. Los átomos de flúor también pueden acoplarse entre sí. Entre átomos de flúor, las constantes de acoplamiento homonuclear son mucho mayores que con átomos de hidrógeno. Los flúor geminales suelen tener un valor J de 250-300 Hz. [11] Hay muchas buenas referencias para valores de constantes de acoplamiento. [11] Las citas se incluyen a continuación.
Imágenes por resonancia magnética
La resonancia magnética con 19 F es una alternativa viable a la resonancia magnética con 1 H. Los problemas de sensibilidad se pueden superar utilizando nanopartículas blandas. Las aplicaciones incluyen agentes de contraste sensibles al pH, la temperatura, las enzimas, los iones metálicos y el rédox . También se pueden utilizar para el marcaje de células a largo plazo. [12]
Notas
Referencias
- ^ Claridge, Timothy (2016). Técnicas de RMN de alta resolución en química orgánica . Oxford, Reino Unido: Elsevier. pp. 428–429. ISBN 978-0-08-099986-9.
- ^ Martino, R.; Gilard, V.; Malet-Martino, M. (2008). Espectroscopia de RMN en análisis farmacéutico . Boston: Elsevier. pág. 371. ISBN 978-0-444-53173-5.
- ^ H. Friebolin "Espectroscopia básica de RMN unidimensional y bidimensional", Wiley-VCH, Weinheim, 2011. ISBN 978-3-527-32782-9
- ^ Harris, Robin Kingsley; Mann, Brian E. RMN y la tabla periódica . p. 13. ISBN 0123276500.
- ^ abcdefgh Rosenau, Carl Philipp; Jelier, Benson J.; Gossert, Alvar D.; Togni, Antonio (16 de mayo de 2018). "Exponiendo los orígenes de la irreproducibilidad en la espectroscopia de RMN de flúor". Angewandte Chemie International Edition . 57 (30): 9528–9533. doi :10.1002/anie.201802620. ISSN 1433-7851. PMID 29663671.
- ^ Harris, RK (2001). "Nomenclatura de RMN. Propiedades de espín nuclear y convenciones para desplazamientos químicos (Recomendaciones de la IUPAC 2001)". Química pura y aplicada . 73 (11): 1795–1818. doi : 10.1351/pac200173111795 .
- ^ H., Dungan, Claude (1970). Recopilación de los desplazamientos químicos de RMN de F19 informados, desde 1951 hasta mediados de 1967. Van Wazer, John R. Nueva York: Wiley-Interscience. ISBN 0471226505.OCLC 88883 .
{{cite book}}: CS1 maint: varios nombres: lista de autores ( enlace ) - ^ ab Silverstein, Robert M.; Webster, Francis X.; Kiemle, David J. (2005). Identificación espectrométrica de compuestos orgánicos (7.ª ed.). Hoboken, NJ: John Wiley & Sons, Inc., págs. 323–326. ISBN 978-0-471-39362-7.
- ^ Jetton, RE; Nanney, JR; Mahaffy, CAL La predicción de las posiciones de la señal de RMN de 19 F de fluoroalquenos utilizando métodos estadísticos, J. Fluorine Chem. 1995 , 72 , 121.
- ^ abc Pretsch, Ernö; Bühlmann, Philippe; Badertscher, Martin (2009). Determinación de la estructura de compuestos orgánicos (4.ª ed.). Berlín, Alemania: Springer. pp. 243–259. ISBN 978-3-540-93809-5.
- ^ abc Dolbier, WR (2009) Una descripción general de la RMN de flúor, en Guía de RMN de flúor para químicos orgánicos, John Wiley & Sons, Inc., Hoboken, NJ, EE. UU. doi : 10.1002/9780470483404.ch2.
- ^ Hermann, Petr; Blahut, Jan; Kotek, Jan; Herynek, Vit (2021). "Capítulo 8. Sondas de iones metálicos paramagnéticos para imágenes por resonancia magnética de 19 F". Iones metálicos en técnicas de bioimagen . Springer. págs. doi :10.1515/9783110685701-014. S2CID 233704089.
![{\displaystyle \delta _{C=CF}~[{\text{ppm}}]=-133,9+Z_{\text{cis}}+Z_{\text{trans}}+Z_{\text{gem}}+S_{\text{cis/trans}}+S_{\text{cis/gem}}+S_{\text{trans/gem}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0bd15cd7307871c6929df108721d783923f17c1a)
![{\displaystyle \delta _{F}~[{\text{ppm}}]=-113.9+\Sigma Z_{\text{orto}}+\Sigma Z_{\text{meta}}+\Sigma Z_{\ texto{para}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aba530dbee85e060a55eaca5f855441a8392eb23)