Cromatografía en columna

La cromatografía en columna en química es un método cromatográfico utilizado para aislar un único compuesto químico de una mezcla. La cromatografía es capaz de separar sustancias basándose en la absorción diferencial de compuestos por el adsorbente; los compuestos se mueven a través de la columna a diferentes velocidades, lo que permite separarlos en fracciones. La técnica es ampliamente aplicable, ya que se pueden utilizar muchos adsorbentes diferentes (fase normal, fase reversa o de otro tipo) con una amplia gama de disolventes. La técnica se puede utilizar en escalas desde microgramos hasta kilogramos. La principal ventaja de la cromatografía en columna es el costo relativamente bajo y la posibilidad de desechar la fase estacionaria utilizada en el proceso. Esto último evita la contaminación cruzada y la degradación de la fase estacionaria debido al reciclaje. La cromatografía en columna se puede realizar utilizando la gravedad para mover el disolvente o utilizando gas comprimido para empujar el disolvente a través de la columna.
Un cromatógrafo de capa fina puede mostrar cómo se comportará una mezcla de compuestos cuando se purifique mediante cromatografía en columna. La separación se optimiza primero mediante cromatografía de capa fina antes de realizar la cromatografía en columna.
Preparación de la columna
Una columna se prepara colocando un adsorbente sólido en un tubo cilíndrico de vidrio o plástico. El tamaño dependerá de la cantidad de compuesto que se vaya a aislar. La base del tubo contiene un filtro, ya sea un tapón de algodón o lana de vidrio, o frita de vidrio para mantener la fase sólida en su lugar. Se puede colocar un depósito de disolvente en la parte superior de la columna.
En general, se utilizan dos métodos para preparar una columna: el método seco y el método húmedo. En el método seco, primero se llena la columna con polvo de fase estacionaria seco, seguido de la adición de fase móvil, que se hace pasar por la columna hasta que esté completamente húmeda y, a partir de este punto, nunca se permite que se seque. [1] En el método húmedo, se prepara una suspensión del eluyente con el polvo de fase estacionaria y luego se vierte con cuidado en la columna. La parte superior de la sílice debe ser plana y se puede proteger con una capa de arena. El eluyente pasa lentamente por la columna para hacer avanzar el material orgánico.
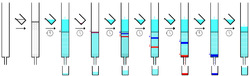
Los componentes individuales son retenidos por la fase estacionaria de manera diferente y se separan entre sí mientras corren a diferentes velocidades a través de la columna con el eluyente. Al final de la columna eluyen uno a la vez. Durante todo el proceso de cromatografía, el eluyente se recoge en una serie de fracciones . Las fracciones se pueden recoger automáticamente por medio de colectores de fracciones. La productividad de la cromatografía se puede aumentar haciendo funcionar varias columnas a la vez. En este caso, se utilizan colectores de múltiples corrientes. La composición del flujo de eluyente se puede monitorear y cada fracción se analiza para compuestos disueltos, por ejemplo, mediante cromatografía analítica, espectros de absorción UV o fluorescencia . Los compuestos coloreados (o compuestos fluorescentes con la ayuda de una lámpara UV) se pueden ver a través de la pared de vidrio como bandas móviles.
Fase estacionaria

La fase estacionaria o adsorbente en la cromatografía en columna es un sólido. La fase estacionaria más común para la cromatografía en columna es el gel de sílice , seguida por la alúmina . En el pasado, se ha utilizado con frecuencia polvo de celulosa . Existe una amplia gama de fases estacionarias disponibles para realizar cromatografía de intercambio iónico , cromatografía de fase inversa (RP), cromatografía de afinidad o adsorción en lecho expandido (EBA). Las fases estacionarias suelen ser polvos o geles finamente molidos y/o son microporosas para una mayor superficie, aunque en la EBA se utiliza un lecho fluidizado. Existe una relación importante entre el peso de la fase estacionaria y el peso seco de la mezcla de analitos que se puede aplicar a la columna. Para la cromatografía en columna de sílice, esta relación se encuentra entre 20:1 y 100:1, dependiendo de qué tan cerca uno del otro se eluyan los componentes del analito. [2]
Fase móvil (eluyente)
La fase móvil o eluyente es un disolvente o una mezcla de disolventes utilizados para mover los compuestos a través de la columna. Se elige de modo que el valor del factor de retención del compuesto de interés sea aproximadamente de alrededor de 0,2 - 0,3 para minimizar el tiempo y la cantidad de eluyente para ejecutar la cromatografía. El eluyente también se ha elegido de modo que los diferentes compuestos se puedan separar de manera efectiva. El eluyente se optimiza en pruebas previas a pequeña escala, a menudo utilizando cromatografía de capa fina (TLC) con la misma fase estacionaria, utilizando disolventes de diferente polaridad hasta que se encuentra un sistema de disolventes adecuado. Los disolventes de fase móvil comunes, en orden de polaridad creciente, incluyen hexano , diclorometano , acetato de etilo , acetona y metanol . [3] Un sistema de disolventes común es una mezcla de hexano y acetato de etilo, con proporciones ajustadas hasta que el compuesto objetivo tenga un factor de retención de 0,2 - 0,3. Contrariamente a la idea errónea común, el metanol solo puede usarse como eluyente para compuestos altamente polares y no disuelve el gel de sílice.
Existe un caudal óptimo para cada separación particular. Un caudal más rápido del eluyente minimiza el tiempo necesario para hacer funcionar una columna y, por lo tanto, minimiza la difusión, lo que da como resultado una mejor separación. Sin embargo, el caudal máximo está limitado porque se requiere un tiempo finito para que el analito se equilibre entre la fase estacionaria y la fase móvil, consulte la ecuación de Van Deemter . Una columna de laboratorio simple funciona por flujo por gravedad . El caudal de una columna de este tipo se puede aumentar extendiendo la columna llena de eluyente fresco por encima de la parte superior de la fase estacionaria o disminuir mediante los controles del grifo. Se pueden lograr caudales más rápidos utilizando una bomba o utilizando gas comprimido (por ejemplo, aire, nitrógeno o argón ) para empujar el disolvente a través de la columna (cromatografía en columna flash). [4] [5]

El tamaño de partícula de la fase estacionaria es generalmente más fino en la cromatografía en columna flash que en la cromatografía en columna de gravedad. Por ejemplo, uno de los grados de gel de sílice más utilizados en la primera técnica es el de malla 230 – 400 (40 – 63 μm), mientras que la segunda técnica requiere típicamente un gel de sílice de malla 70 – 230 (63 – 200 μm). [6]
Se ha desarrollado una hoja de cálculo que ayuda al desarrollo exitoso de columnas flash. La hoja de cálculo estima el volumen de retención y el volumen de banda de los analitos, los números de fracción que se espera que contenga cada analito y la resolución entre picos adyacentes. Esta información permite a los usuarios seleccionar parámetros óptimos para separaciones a escala preparativa antes de intentar la propia columna flash. [7]
Sistemas automatizados

La cromatografía en columna es una etapa que consume mucho tiempo en cualquier laboratorio y puede convertirse rápidamente en un cuello de botella para cualquier laboratorio de procesos. Muchos fabricantes como Biotage, Buchi, Interchim y Teledyne Isco han desarrollado sistemas de cromatografía flash automatizados (normalmente denominados LPLC, cromatografía líquida de baja presión, alrededor de 350–525 kPa o 50,8–76,1 psi) que minimizan la participación humana en el proceso de purificación. Los sistemas automatizados incluirán componentes que normalmente se encuentran en sistemas de cromatografía líquida de alto rendimiento (HPLC) más caros, como una bomba de gradiente, puertos de inyección de muestra, un detector UV y un colector de fracciones para recoger el eluyente. Normalmente, estos sistemas automatizados pueden separar muestras desde unos pocos miligramos hasta una escala industrial de muchos kilogramos y ofrecen una solución mucho más barata y rápida que realizar inyecciones múltiples en sistemas de HPLC preparativos.
La resolución (o la capacidad de separar una mezcla) en un sistema LPLC siempre será menor en comparación con la HPLC, ya que el material de relleno en una columna HPLC puede ser mucho más pequeño, típicamente solo 5 micrómetros, lo que aumenta el área de superficie de la fase estacionaria, aumenta las interacciones de la superficie y brinda una mejor separación. Sin embargo, el uso de este pequeño medio de relleno causa la alta contrapresión y es por eso que se denomina cromatografía líquida de alta presión. Las columnas LPLC generalmente están rellenas con sílice de alrededor de 50 micrómetros, lo que reduce la contrapresión y la resolución, pero también elimina la necesidad de costosas bombas de alta presión. Los fabricantes ahora están comenzando a avanzar hacia sistemas de cromatografía flash de mayor presión y los han denominado sistemas de cromatografía líquida de presión media (MPLC) que operan por encima de 1 MPa (150 psi).
Cálculo de la resolución del cromatograma de columna

Por lo general, la cromatografía en columna se realiza con bombas peristálticas, haciendo fluir los tampones y la muestra de solución por la parte superior de la columna. Las soluciones y los tampones pasan por la columna, donde un colector de fracciones al final de la configuración de la columna recoge las muestras eluidas. Antes de la recogida de fracciones, las muestras que se eluyen de la columna pasan por un detector, como un espectrofotómetro o un espectrómetro de masas, de modo que se pueda determinar la concentración de las muestras separadas en la mezcla de solución de muestra.
Por ejemplo, si se quisiera separar dos proteínas diferentes con distintas capacidades de unión a la columna a partir de una muestra de solución, un buen tipo de detector sería un espectrofotómetro que utilice una longitud de onda de 280 nm. Cuanto mayor sea la concentración de proteína que pasa a través de la solución eluida a través de la columna, mayor será la absorbancia de esa longitud de onda.
Debido a que la cromatografía en columna tiene un flujo constante de solución eluida que pasa a través del detector en concentraciones variables, el detector debe representar gráficamente la concentración de la muestra eluida a lo largo del tiempo. Este gráfico de la concentración de la muestra en función del tiempo se denomina cromatograma.
El objetivo final de la cromatografía es separar los diferentes componentes de una mezcla de soluciones. La resolución expresa el grado de separación entre los componentes de la mezcla. Cuanto mayor sea la resolución del cromatograma, mejor será el grado de separación de las muestras que proporciona la columna. Estos datos son una buena forma de determinar las propiedades de separación de la columna de esa muestra en particular. La resolución se puede calcular a partir del cromatograma.
Las curvas separadas en el diagrama representan diferentes perfiles de concentración de elución de la muestra a lo largo del tiempo en función de su afinidad con la resina de la columna. Para calcular la resolución, se requieren el tiempo de retención y el ancho de la curva.
El tiempo de retención es el tiempo transcurrido desde el inicio de la detección de la señal por parte del detector hasta la altura máxima del perfil de concentración de elución de cada muestra diferente.
El ancho de la curva es el ancho de la curva del perfil de concentración de las diferentes muestras en el cromatograma en unidades de tiempo.
Un método simplificado para calcular la resolución del cromatograma consiste en utilizar el modelo de placas. [8] El modelo de placas supone que la columna se puede dividir en un número determinado de secciones o placas y que se puede calcular el balance de masa para cada placa individual. Este enfoque aproxima una curva de cromatograma típica como una curva de distribución gaussiana . Al hacer esto, el ancho de la curva se estima como 4 veces la desviación estándar de la curva, 4σ. El tiempo de retención es el tiempo desde el inicio de la detección de la señal hasta el momento de la altura del pico de la curva gaussiana.
A partir de las variables de la figura anterior, la resolución, el número de placa y la altura de placa del modelo de placa de columna se pueden calcular utilizando las ecuaciones:
Resolución (R s ):
- R s = 2(t RB – t RA )/(w B + w A ),
dónde:
- tRB = tiempo de retención del soluto B
- t RA = tiempo de retención del soluto A
- w B = Ancho de la curva gaussiana del soluto B
- w A = ancho de la curva gaussiana del soluto A
Número de placa (N):
- N = (t R ) 2 /(w/4) 2
Altura de la placa (H):
- H = L/N
donde L es la longitud de la columna. [8]
Equilibrio de adsorción en columna
En una columna de adsorción, la resina de la columna (fase estacionaria) está compuesta de microesferas. Incluso partículas más pequeñas, como proteínas, carbohidratos, iones metálicos u otros compuestos químicos, se conjugan con las microesferas. Se puede suponer que cada partícula de unión que está adherida a la microesfera se une en una proporción de 1:1 con la muestra de soluto enviada a través de la columna que necesita purificarse o separarse.
La unión entre la molécula objetivo a separar y la molécula de unión en las perlas de la columna se puede modelar utilizando una reacción de equilibrio simple K eq = [CS]/([C][S]) donde K eq es la constante de equilibrio , [C] y [S] son las concentraciones de la molécula objetivo y la molécula de unión en la resina de la columna, respectivamente. [CS] es la concentración del complejo de la molécula objetivo unida a la resina de la columna. [8]
Utilizando esto como base, se pueden utilizar tres isotermas diferentes para describir la dinámica de unión de una cromatografía en columna: lineal, Langmuir y Freundlich.
La isoterma lineal se produce cuando la concentración de soluto que se necesita purificar es muy pequeña en relación con la molécula de unión. Por lo tanto, el equilibrio se puede definir como:
- [CS] = K eq [C].
Para usos a escala industrial, se deben tener en cuenta las moléculas de unión totales en las perlas de resina de la columna, ya que se deben tener en cuenta los sitios desocupados. La isoterma de Langmuir y la isoterma de Freundlich son útiles para describir este equilibrio. La isoterma de Langmuir se expresa mediante:
- [CS] = (K eq S tot [C])/(1 + K eq [C]), donde S tot es la cantidad total de moléculas de unión en las perlas.
La isoterma de Freundlich viene dada por:
- [CS] = K equivalente [C] 1/n
La isoterma de Freundlich se utiliza cuando la columna puede unirse a muchas muestras diferentes en la solución que necesita purificarse. Debido a que las muchas muestras diferentes tienen constantes de unión diferentes a las perlas, existen muchas ecuaciones K diferentes . Por lo tanto, la isoterma de Langmuir no es un buen modelo para la unión en este caso. [8]
Véase también
- Cromatografía líquida rápida de proteínas (FPLC): separación de proteínas mediante cromatografía en columna
- Cromatografía líquida de alto rendimiento (HPLC): cromatografía en columna que utiliza alta presión
Referencias
- ^ Shusterman, AJ; McDougal, PG; Glasfeld, A (1997). "Cromatografía flash en columna seca". J Chem Educ . 74 (10): 1222. Bibcode :1997JChEd..74.1222S. doi :10.1021/ed074p1222. ISSN 0021-9584.
- ^ "Cómo configurar una columna de sílice para cromatografía flash y lograr una separación exitosa". reachdevices.com . REACH Devices, LLC . Consultado el 3 de enero de 2019 .
- ^ Furniss, Brian S.; Hannaford, Antony, J.; Smith, Peter WG; Tatchell, Austin S. (1989). Libro de texto de química orgánica práctica de Vogel . Longman Scientific & Technical. pág. 203. ISBN 978-0582462366.
{{cite book}}: CS1 maint: varios nombres: lista de autores ( enlace ) - ^ Still, WC; Kahn, M; Mitra, A (1978). "Técnica cromatográfica rápida para separaciones preparativas con resolución moderada". J Org Chem . 43 (14). ACS : 2923–2925. doi :10.1021/jo00408a041.
- ^ Harwood LM, Moody CJ (13 de junio de 1989). Química orgánica experimental: principios y práctica (edición ilustrada). Londres: Blackwell. pp. 180–185. ISBN 978-0-632-02017-1.OCLC 1079261960 .
- ^ "Material Harvest Silica Gel for Normal Phase Column Chromatography" (Gel de sílice de Material Harvest para cromatografía en columna de fase normal). Material Harvest. 2008. Consultado el 3 de enero de 2019 .
- ^ Fair, JD; Kormos, CM (2008). "Cromatogramas de columna flash estimados a partir de datos de cromatografía de capa fina". J Chromatogr A . 1211 (1–2): 49–54. doi :10.1016/j.chroma.2008.09.085. ISSN 0021-9673. PMID 18849041.
- ^ abcd Harrison RG, Todd PW, Rudge SR, Petrides DP (2003). Ciencia e ingeniería de bioseparaciones (2.ª ed.). Nueva York, NY: Oxford University Press . ISBN 9780190213732.OCLC 899240244 .
Enlaces externos
- Guía de cromatografía en columna flash (pdf)
- Cromatografía de flujo radial