Célula P19
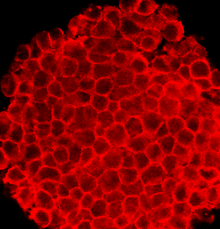
Las células P19 son una línea celular de carcinoma embrionario derivada de un teratocarcinoma derivado de embriones en ratones. La línea celular es pluripotente y puede diferenciarse en tipos celulares de las tres capas germinales. Además, es la línea celular de carcinoma embrionario (CE) más caracterizada que puede inducirse en células musculares cardíacas y células neuronales mediante diferentes tratamientos específicos. De hecho, la exposición de células P19 agregadas a dimetilsulfóxido (DMSO) induce la diferenciación en músculo cardíaco y esquelético . Además, la exposición de células P19 al ácido retinoico (AR) puede diferenciarlas en células neuronales. [1]
Origen de la línea celular P19
Las células cancerosas en humanos pueden provocar la muerte del paciente si la célula cancerosa agresiva crece y hace metástasis. Sin embargo, los investigadores utilizan estas células para estudiar el desarrollo de las células cancerosas con el fin de encontrar tratamientos más específicos. Para los biólogos del desarrollo, el carcinoma embrionario , que se deriva del teratocarcinoma, es un buen objeto de estudio del desarrollo. En 1982, McBurney y Rogers trasplantaron un embrión de ratón de 7,5 días en el testículo para inducir el crecimiento del tumor. Se aislaron cultivos celulares que contenían células madre indiferenciadas del tumor primario que tienen un cariotipo euploide . Estas células madre se denominaron células de carcinoma embrionario P19. [2] Estas células P19 derivadas crecieron rápidamente sin células alimentadoras y fueron fáciles de mantener. Además, la multipotencia de las células P19 se confirmó luego inyectando las células en blastocistos de otra cepa de ratón. Los investigadores descubrieron que había tejidos de las tres capas germinales creciendo en el ratón receptor. [3] Basándose en sus estudios continuos, derivaron además líneas celulares de subtipos a partir de células P19 originales: P19S18, P19D3, P19RAC65 y P19C16. La diferencia entre estas líneas celulares de subtipos es la capacidad de diferenciarse en células neuronales o células musculares en respuesta al tratamiento con ácido retinoico o DMSO, respectivamente. [3] [4] [5] Más recientemente, varios estudios generan líneas celulares que inicialmente se derivaron de células P19 diferenciadas. Debido a la pluripotencia de las células P19, esas nuevas líneas celulares derivadas pueden ser células similares al ectodermo , mesodermo y endodermo . [6]
Diferenciación de células P19
Las células P19 pueden mantenerse en crecimiento exponencial debido a una composición cromosómica estable. Debido a que el carcinoma embrionario puede diferenciarse en células de las tres capas germinales, las células P19 también pueden diferenciarse en células similares al ectodermo, mesodermo y endodermo. Cuando las células de carcinoma embrionario se cultivan a alta densidad, comienzan a diferenciarse. [7] Al agregar las células en un cuerpo embrionario, las células EC también pueden procesar la diferenciación. [8] En las células P19, la adición de concentraciones no tóxicas de fármacos a las células del cuerpo embrionario agregadas puede inducir la diferenciación de las células P19 en líneas celulares específicas según el fármaco añadido. [1] Los dos fármacos más comunes y eficaces son el ácido retinoico (RA) y el dimetilsulfóxido (DMSO). Los estudios han demostrado que una determinada concentración de RA puede inducir a las células P19 a diferenciarse en células neuronales, incluidas las neuronas y las células gliales , [9] mientras que el 0,5% - 1% de DMSO llevó a las células P19 a diferenciarse en células musculares cardíacas o esqueléticas. En el método de tratamiento de AR, las neuronas, la astroglia y los fibroblastos se pueden identificar después de la agregación. Las células diferenciadas también tienen actividades de colina acetiltransferasa y acetilcolinesterasa. [10] Cuando se trató con DMSO, las células del músculo cardíaco se desarrollaron después de 5 días de exposición y las células del músculo esquelético aparecieron después de 8 días de exposición. Esos estudios mostraron que la exposición al fármaco hace que las células P19 multipotentes se diferencien en diferentes capas de células. Debido a que la concentración de ácido retinoico o DMSO no es tóxica para las células, la diferenciación específica del fármaco se debe a la inducción de células, no a la selección. Se han generado mutantes de células P19 para investigar el mecanismo de diferenciación específica del fármaco. [10] Además, también se investigaron las vías de señalización relacionadas con la neurogénesis y la miogénesis estudiando la expresión genética o generando mutantes de células P19.
Neurogénesis en células P19.
El tratamiento de células P19 indiferenciadas con ácido retinoico puede inducirlas específicamente a convertirse en células neuronales. El uso de dosis entre 1 μM y 3 μM de AR puede generar neuronas como el tipo celular más abundante. [4]
Las neuronas bajo este tratamiento alcanzaron las poblaciones más altas entre seis y nueve días. Varios marcadores neuronales como las proteínas de neurofilamento , el antígeno HNK-1 y los sitios de unión de la toxina del tétano se expresan en niveles más altos durante estos días. [11]
Después de seis a nueve días de tratamiento, la población neuronal relativa disminuye, probablemente debido a una proliferación más rápida de células no neuronales. Después de 10 días de exposición, las células astrogliales se pueden detectar utilizando la proteína ácida fibrilar glial (GFAP), que es un marcador específico de las células gliales. Además de las neuronas y los astrocitos , las células P19 también pueden diferenciarse en oligodendrocitos , que pueden detectarse utilizando los marcadores específicos, la glicoproteína asociada a la mielina y la 2',3'-nucleótido cíclico 3'-fosfodiesterasa . Además, los oligodendrocitos también se desarrollaron y migraron en haces de fibras en ratones cuando las células inducidas por AR se trasplantaron en los cerebros . [12]
El ácido retinoico puede inducir no solo la diferenciación de las células P19 sino también de otras células progenitoras o células madre embrionarias . Dado que las células después del tratamiento con ácido retinoico no expresaron inmediatamente genes marcadores neuronales, la AR debe iniciar alguna vía para procesar la diferenciación celular. Muchos estudios utilizaron células P19 para investigar los mecanismos inducidos por la AR, incluida la generación del alelo mutante de los genes del receptor de ácido retinoico y el estudio de la expresión de los genes del receptor, los genes Hox y las proteínas de unión al retinol mientras se exponían a la AR. [13] [14]
Todos estos estudios indican que la célula P19 es un buen sistema modelo in vitro para investigar el mecanismo de los fármacos que interfieren con una vía celular específica. Además, al utilizar la capacidad de la neurogénesis inducida por AR en la célula P19, muchos investigadores comenzaron a identificar los mecanismos de diferenciación in vitro de la neurogénesis o la gliogénesis. Se investigan varias vías relacionadas, como la vía Wnt/β-catenina, la vía Notch y la vía hedgehog , ya sea mediante la expresión génica o generando alelos para genes relacionados. [15] [16] [17]
Miogénesis en la línea celular P19
Al igual que el ácido retinoico, la diferenciación inducida por DMSO no es específica de las células P19. También podría inducir células de neuroblastoma , células de cáncer de pulmón y células ES de ratón. [18] [19] [20] En una concentración de 0,5-1%, DMSO indujo a las células P19 a agregarse y procesar tipos de células mesodérmicas y endodérmicas. [1] [10] [21]
El mecanismo celular que ocurre durante la agregación y la diferenciación aún no se ha estudiado por completo. Sin embargo, algunos estudios mostraron que la comunicación celular juega un papel importante en la diferenciación muscular en las células P19, lo que podría explicar por qué las células necesitan agregarse primero para procesar la diferenciación muscular. [6]
Para dilucidar el mecanismo de miogénesis en las células P19, se encontró que varios factores de transcripción específicos cardíacos , incluidos GATA-4, MEF2c, Msx-1, Nkx2.5, MHox, Msx-2 y MLP, cambian durante la diferenciación. [6] Los informes han demostrado que GATA-4, NKx2.5 y MEF2c se regularon positivamente después de la inducción con DMSO. [22] [23] En los últimos años, las células P19 también se utilizaron para estudiar el mecanismo de diferenciación cardíaca y miogénesis. La principal vía de señalización afectada , la vía de las proteínas morfogenéticas óseas (BMP), es la señalización más estudiada en las células P19. Al generar la línea celular P19CL6noggin, que sobreexpresa el antagonista de BMP noggin , descubrieron que las células mutantes no se diferenciaban en cardiomiocitos cuando se trataban con 1% de DMSO, lo que sugiere que las BMP eran indispensables para la diferenciación de cardiomiocitos en este sistema. También proporcionaron la evidencia que muestra que TAK1, Nkx-2.5 y GATA-4 son importantes en la vía de señalización cardiogénica de BMP. [24]
Direcciones futuras
Las células P19 proporcionan una valiosa formación de células neuronales y musculares in vitro. Dado que las células P19 son fáciles de mantener y cultivar en comparación con otras células madre embrionarias, son un modelo conveniente para realizar estudios de desarrollo in vitro. Las técnicas para manipular esta línea celular para expresar o inactivar ciertos genes permiten una investigación detallada de las vías de señalización, los aspectos funcionales y la regulación de la expresión de proteínas de la miogénesis y la neurogénesis. La investigación ampliada también puede dilucidar las etapas posteriores del desarrollo y la maduración del corazón o el cerebro .
Referencias
- ^ abc McBurney, MW; Rogers, BJ (febrero de 1982). "Aislamiento de células de carcinoma embrionario masculino y sus patrones de replicación cromosómica". Biología del desarrollo . 89 (2): 503–8. doi :10.1016/0012-1606(82)90338-4. PMID 7056443.
- ^ McBurney, MW (1993). "Células de carcinoma embrionario P19". Int J Dev Biol . 37 (1): 135–140. PMID 8507558.
- ^ ab Rossant, J; McBurney, MW (agosto de 1982). "El potencial de desarrollo de una línea celular euploide de teratocarcinoma masculino después de la inyección de blastocisto". Revista de embriología y morfología experimental . 70 : 99–112. PMID 7142904.
- ^ ab Fahnestock, M; Koshland DE, Jr (febrero de 1979). "Control del receptor de los taxis de galactosa en Salmonella typhimurium". Journal of Bacteriology . 137 (2): 758–63. doi :10.1128/jb.137.2.758-763.1979. PMC 218354 . PMID 370099.
- ^ Craine, BL; Rupert, CS (febrero de 1979). "Interacciones entre el ácido desoxirribonucleico y la membrana cerca del origen de replicación e inicio de la síntesis del ácido desoxirribonucleico en Escherichia coli". Journal of Bacteriology . 137 (2): 740–5. doi :10.1128/jb.137.2.740-745.1979. PMC 218351 . PMID 370098.
- ^ abc van der Heyden, MA; Defize, LH (1 de mayo de 2003). "Veintiún años de células P19: lo que nos enseñó una línea celular de carcinoma embrionario sobre la diferenciación de los cardiomiocitos". Investigación cardiovascular . 58 (2): 292–302. doi : 10.1016/S0008-6363(02)00771-X . PMID 12757864.
- ^ McBurney, MW (noviembre de 1976). "Líneas clonales de células de teratocarcinoma in vitro: diferenciación y características citogenéticas". Journal of Cellular Physiology . 89 (3): 441–55. doi :10.1002/jcp.1040890310. PMID 988033.
- ^ Martin, GR; Evans MJ (1975). "Diferenciación múltiple de células madre de teratocarcinoma clonal tras la formación del cuerpo embrionario in vitro". Cell . 6 (4): 467–74. doi :10.1016/0092-8674(75)90035-5.
- ^ Edwards, MK; Harris, JF; McBurney, MW (diciembre de 1983). "Diferenciación muscular inducida en una línea celular de carcinoma embrionario". Biología molecular y celular . 3 (12): 2280–6. doi :10.1128/mcb.3.12.2280. PMC 370099 . PMID 6656767.
- ^ abc Jones-Villeneuve, EM; Rudnicki, MA; Harris, JF; McBurney, MW (diciembre de 1983). "Diferenciación neural inducida por ácido retinoico de células de carcinoma embrionario". Biología molecular y celular . 3 (12): 2271–9. doi :10.1128/mcb.3.12.2271. PMC 370098 . PMID 6656766.
- ^ McBurney, MW; Reuhl, KR; Ally, AI; Nasipuri, S; Bell, JC; Craig, J (marzo de 1988). "Diferenciación y maduración de neuronas derivadas de carcinoma embrionario en cultivo celular". The Journal of Neuroscience . 8 (3): 1063–73. doi : 10.1523/JNEUROSCI.08-03-01063.1988 . PMC 6569242 . PMID 2894413.
- ^ Staines, WA; Craig, J; Reuhl, K; McBurney, MW (abril de 1996). "Las células de carcinoma embrionario P19 tratadas con ácido retinoico se diferencian en oligodendrocitos capaces de mielinizarse". Neuroscience . 71 (3): 845–53. doi :10.1016/0306-4522(95)00494-7. PMID 8867053.
- ^ Pratt, MA; Kralova, J; McBurney, MW (diciembre de 1990). "Una mutación negativa dominante del gen del receptor de ácido retinoico alfa en una célula de carcinoma embrionario que no responde al ácido retinoico". Biología molecular y celular . 10 (12): 6445–53. doi :10.1128/mcb.10.12.6445. PMC 362921 . PMID 2174108.
- ^ Chen, Y; Reese, DH (octubre de 2011). "La vía de señalización del retinol en células P19 pluripotentes de ratón". Journal of Cellular Biochemistry . 112 (10): 2865–72. doi :10.1002/jcb.23200. PMID 21618588.
- ^ Nye, JS; Kopan, R; Axel, R (septiembre de 1994). "Un Notch activado suprime la neurogénesis y la miogénesis, pero no la gliogénesis, en células de mamíferos". Desarrollo . 120 (9): 2421–30. doi :10.1242/dev.120.9.2421. PMID 7956822.
- ^ Hamada-Kanazawa, M; Ishikawa, K; Nomoto, K; Uozumi, T; Kawai, Y; Narahara, M; Miyake, M (2004-02-27). "La sobreexpresión de Sox6 provoca la agregación celular y la diferenciación neuronal de las células de carcinoma embrionario P19 en ausencia de ácido retinoico". FEBS Letters . 560 (1–3): 192–8. Bibcode :2004FEBSL.560..192H. doi : 10.1016/S0014-5793(04)00086-9 . PMID 14988021.
- ^ Tan, Y; Xie, Z; Ding, M; Wang, Z; Yu, Q; Meng, L; Zhu, H; Huang, X; Yu, L; Meng, X; Chen, Y (septiembre de 2010). "Los niveles aumentados del factor de transcripción FoxA1 en células de carcinoma embrionario pluripotente P19 estimulan la diferenciación neuronal". Células madre y desarrollo . 19 (9): 1365–74. doi :10.1089/scd.2009.0386. PMID 19916800.
- ^ Lako, M; Lindsay, S; Lincoln, J; Cairns, PM; Armstrong, L; Hole, N (2001). "Caracterización de la expresión del gen Wnt durante la diferenciación de células madre embrionarias murinas in vitro: papel de Wnt3 en la mejora de la diferenciación hematopoyética". Mecanismos del desarrollo . 103 (1–2): 49–59. doi : 10.1016/S0925-4773(01)00331-8 . PMID 11335111.
- ^ Tralka, TS; Rabson, AS (diciembre de 1976). "Formación de cilios en cultivos de células de cáncer de pulmón humano tratadas con dimetilsulfóxido". Journal of the National Cancer Institute . 57 (6): 1383–8. doi :10.1093/jnci/57.6.1383. PMID 1003564.
- ^ Littauer, UZ; Palfrey, C; Kimhi, Y; Spector, I (mayo de 1978). "Inducción de la diferenciación en células de neuroblastoma de ratón". Monografía del Instituto Nacional del Cáncer (48): 333–7. PMID 748753.
- ^ McBurney, MW; Jones-Villeneuve, EM; Edwards, MK; Anderson, PJ (9 de septiembre de 1982). "Control de la diferenciación muscular y neuronal en una línea celular de carcinoma embrionario cultivada". Nature . 299 (5879): 165–7. Bibcode :1982Natur.299..165M. doi :10.1038/299165a0. PMID 7110336.Después de 2 días de exposición, aparecieron células similares al endodermo que se asemejaban al endodermo extraembrionario primitivo. Después de 6 días de exposición, apareció el músculo cardíaco en el interior de los agregados. El contenido de células musculares cardíacas fue del 25% de las células. Después de 10 días de exposición, aparecieron células musculares esqueléticas alrededor del cuerpo del embrión.
- ^ Skerjanc, IS; Petropoulos, H; Ridgeway, AG; Wilton, S (25 de diciembre de 1998). "El factor potenciador de miocitos 2C y Nkx2-5 regulan positivamente la expresión del otro e inician la cardiomiogénesis en células P19". The Journal of Biological Chemistry . 273 (52): 34904–10. doi : 10.1074/jbc.273.52.34904 . PMID 9857019.
- ^ Grépin, C; Nemer, G; Nemer, M (junio de 1997). "Cardiogénesis mejorada en células madre embrionarias que sobreexpresan el factor de transcripción GATA-4". Desarrollo . 124 (12): 2387–95. doi :10.1242/dev.124.12.2387. PMID 9199365.
- ^ Monzen, K; Shiojima, I; Hiroi, Y; Kudoh, S; Oka, T; Takimoto, E; Hayashi, D; Hosoda, T; Habara-Ohkubo, A; Nakaoka, T; Fujita, T; Yazaki, Y; Komuro, I (octubre de 1999). "Las proteínas morfogenéticas óseas inducen la diferenciación de cardiomiocitos a través de la proteína quinasa activada por mitógenos TAK1 y los factores de transcripción cardíacos Csx/Nkx-2.5 y GATA-4". Biología molecular y celular . 19 (10): 7096–105. doi :10.1128/mcb.19.10.7096. PMC 84704 . PMID 10490646.
Enlaces externos
- Vanderheyden, M; Defize, L (2003). "Veintiún años de células P19: lo que nos enseñó una línea celular de carcinoma embrionario sobre la diferenciación de los cardiomiocitos". Investigación cardiovascular . 58 (2): 292–302. doi : 10.1016/S0008-6363(02)00771-X . PMID 12757864.
- Entrada de Cellosaurus para P19