August Kekulé
Este artículo necesita citas adicionales para su verificación . ( junio de 2015 ) |
August Kekulé | |
|---|---|
 | |
| Nacido | Federico Augusto Kekulé (1829-09-07)7 de septiembre de 1829 |
| Fallecido | 13 de julio de 1896 (1896-07-13)(66 años) |
| Nacionalidad | Alemán |
| Alma máter | Universidad de Giessen |
| Conocido por | Teoría de la estructura química Tetravalencia del carbono Estructura del benceno |
| Premios | Pour le Mérite (1893) Medalla Copley (1885) ForMemRS (1875) |
| Carrera científica | |
| Instituciones | Universidad de Heidelberg Universidad de Gante Universidad de Bonn |
| Tesis | Ueber die Amyloxydschwefelsäure und einige ihrer Salze (1852) |
| Asesores académicos | Justo de Liebig |
| Estudiantes de doctorado | Jacobus Henricus van 't Hoff Hermann Emil Fischer Adolf von Baeyer Richard Anschütz |
Friedrich August Kekulé , más tarde Friedrich August Kekule von Stradonitz ( / ˈk eɪ k əl eɪ / KAY -kə-lay , [1] alemán: [ˈfʁiːdʁɪç ˈʔaʊɡʊst ˈkeːkuleː fɔn ʃtʁaˈdoːnɪts] ; 7 de septiembre de 1829 - 13 de julio de 1896), fue un químico orgánico alemán . Desde la década de 1850 hasta su muerte, Kekulé fue uno de los químicos más destacados de Europa, especialmente en el campo de la química teórica . Fue el principal fundador de la teoría de la estructura química y en particular de la estructura de Kekulé del benceno .
Nombre
Kekulé nunca utilizó su primer nombre de pila; durante toda su vida fue conocido como August Kekulé. Después de ser ennoblecido por el Káiser en 1895, adoptó el nombre de August Kekule von Stradonitz, sin el acento francés agudo sobre la segunda "e". Al parecer, el acento francés había sido añadido al nombre por el padre de Kekulé durante la ocupación napoleónica de Hesse por Francia, para garantizar que los francófonos pronunciaran la tercera sílaba. [2]
Primeros años
Hijo de un funcionario, Kekulé nació en Darmstadt , capital del Gran Ducado de Hesse . Tras graduarse en la escuela secundaria (el Gimnasio Gran Ducal de Darmstadt), en el otoño de 1847 ingresó en la Universidad de Giessen , con la intención de estudiar arquitectura. [3] Después de escuchar las conferencias de Justus von Liebig en su primer semestre, decidió estudiar química. [3] Tras cuatro años de estudio en Giessen y un breve servicio militar obligatorio, realizó ayudantías temporales en París (1851-1852), en Coira , Suiza (1852-1853) y en Londres (1853-1855), donde recibió una influencia decisiva de Alexander Williamson . Su doctorado en Giessen le fue otorgado en el verano de 1852.
Teoría de la estructura química
En 1856, Kekulé se convirtió en Privatdozent en la Universidad de Heidelberg . En 1858, fue contratado como profesor titular en la Universidad de Gante , luego en 1867 fue llamado a Bonn , donde permaneció por el resto de su carrera. Basando sus ideas en las de predecesores como Williamson, Charles Gerhardt , Edward Frankland , William Odling , Auguste Laurent , Charles-Adolphe Wurtz y otros, Kekulé fue el principal formulador de la teoría de la estructura química (1857-58). Esta teoría procede de la idea de la valencia atómica, especialmente la tetravalencia del carbono (que Kekulé anunció a fines de 1857) [4] y la capacidad de los átomos de carbono para unirse entre sí (anunciada en un artículo publicado en mayo de 1858), [5] hasta la determinación del orden de enlace de todos los átomos en una molécula. Archibald Scott Couper llegó de forma independiente a la idea de la autounión de los átomos de carbono (su artículo apareció en junio de 1858), [6] y proporcionó las primeras fórmulas moleculares donde las líneas simbolizan los enlaces que conectan los átomos. Para los químicos orgánicos, la teoría de la estructura proporcionó una claridad de comprensión dramáticamente nueva y una guía confiable tanto para el trabajo analítico como, especialmente, sintético. Como consecuencia, el campo de la química orgánica se desarrolló explosivamente a partir de este punto. Entre los que fueron más activos en la búsqueda de las primeras investigaciones estructurales se encontraban, además de Kekulé y Couper, Frankland , Wurtz , Alexander Crum Brown , Emil Erlenmeyer y Alexander Butlerov . [7]
La idea de Kekulé de asignar ciertos átomos a ciertas posiciones dentro de la molécula y conectarlos esquemáticamente utilizando lo que él llamó sus "Verwandtschaftseinheiten" ("unidades de afinidad", ahora llamadas " valencias " o "enlaces"), se basó en gran medida en evidencia de reacciones químicas, en lugar de métodos instrumentales que pudieran mirar directamente dentro de la molécula, como la cristalografía de rayos X. Tales métodos físicos de determinación estructural aún no se habían desarrollado, por lo que los químicos de la época de Kekulé tuvieron que confiar casi por completo en la llamada química "húmeda". Algunos químicos, en particular Hermann Kolbe , criticaron duramente el uso de fórmulas estructurales que se ofrecían, según él pensaba, sin prueba. Sin embargo, la mayoría de los químicos siguieron el ejemplo de Kekulé en la búsqueda y desarrollo de lo que algunos han llamado teoría de la estructura "clásica", que fue modificada después del descubrimiento de los electrones (1897) y el desarrollo de la mecánica cuántica (en la década de 1920).
La idea de que el número de valencias de un elemento dado era invariable fue un componente clave de la versión de Kekulé de la química estructural. [8] Esta generalización sufrió muchas excepciones y fue posteriormente reemplazada por la sugerencia de que las valencias estaban fijadas en ciertos estados de oxidación . [9] Por ejemplo, el ácido peryódico según la teoría de la estructura de Kekulé podría representarse por la estructura de cadena IOOOOH. Por el contrario, la estructura moderna del ácido (meta)peryódico tiene los cuatro átomos de oxígeno rodeando al yodo en una geometría tetraédrica. [10]
Benceno
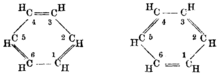
El trabajo más famoso de Kekulé fue sobre la estructura del benceno . [3] En 1865, Kekulé publicó un artículo en francés (porque todavía estaba en Bélgica) sugiriendo que la estructura contenía un anillo de seis miembros de átomos de carbono con enlaces simples y dobles alternados. [11] El año siguiente publicó un artículo mucho más largo en alemán sobre el mismo tema. [12]
La fórmula empírica del benceno se conocía desde hacía mucho tiempo, pero determinar su estructura altamente insaturada era todo un reto. Archibald Scott Couper en 1858 y Joseph Loschmidt en 1861 sugirieron posibles estructuras que contenían múltiples enlaces dobles o múltiples anillos, pero el estudio de los compuestos aromáticos estaba en sus inicios y entonces había muy pocas pruebas disponibles para ayudar a los químicos a decidirse por una estructura en particular.
En 1865 se disponía de más pruebas, especialmente en relación con las relaciones de los isómeros aromáticos . Kekulé defendió su propuesta estructural considerando el número de isómeros observados en los derivados del benceno. Para cada monoderivado del benceno (C 6 H 5 X, donde X = Cl, OH, CH 3 , NH 2 , etc.) solo se encontró un isómero, lo que implica que los seis carbonos son equivalentes, de modo que la sustitución en cualquier carbono da como resultado un único producto posible. Para los diderivados como las toluidinas , C 6 H 4 (NH 2 )(CH 3 ), se observaron tres isómeros, para los que Kekulé propuso estructuras con los dos átomos de carbono sustituidos separados por uno, dos y tres enlaces carbono-carbono, posteriormente denominados isómeros orto, meta y para respectivamente. [13]
Sin embargo, el recuento de posibles isómeros para los diderivados fue criticado por Albert Ladenburg , un ex alumno de Kekulé, quien argumentó que la estructura de Kekulé de 1865 implicaba dos estructuras "orto" distintas, dependiendo de si los carbonos sustituidos están separados por un enlace simple o doble. [14] Dado que los derivados orto del benceno nunca se encontraron en más de una forma isomérica, Kekulé modificó su propuesta en 1872 y sugirió que la molécula de benceno oscila entre dos estructuras equivalentes, de tal manera que los enlaces simples y dobles intercambian posiciones continuamente. [15] [16] Esto implica que los seis enlaces carbono-carbono son equivalentes, ya que cada uno es simple la mitad del tiempo y doble la otra mitad. Una base teórica más firme para una idea similar fue propuesta más tarde en 1928 por Linus Pauling , quien reemplazó la oscilación de Kekulé por el concepto de resonancia entre estructuras mecánico-cuánticas. [17]
El sueño de Kekulé

La nueva comprensión del benceno, y por lo tanto de todos los compuestos aromáticos, resultó ser tan importante tanto para la química pura como para la química aplicada después de 1865 que en 1890 la Sociedad Química Alemana organizó un elaborado homenaje en honor de Kekulé, celebrando el vigésimo quinto aniversario de su primer artículo sobre el benceno. En este acto, Kekulé habló de la creación de la teoría. Dijo que había descubierto la forma de anillo de la molécula de benceno después de haber tenido una ensoñación o ensoñación de una serpiente que se agarraba la cola (se trata de un antiguo símbolo conocido como el uróboros ). [18]
Otra representación del benceno había aparecido en 1886 en el Berichte der Durstigen Chemischen Gesellschaft (Revista de la Sociedad Química Sedienta), una parodia del Berichte der Deutschen Chemischen Gesellschaft , solo que la parodia tenía seis monos agarrándose unos a otros en un círculo, en lugar de una sola serpiente como en la anécdota de Kekulé. [19] Algunos historiadores han sugerido que la parodia era una sátira de la anécdota de la serpiente, posiblemente ya conocida a través de la transmisión oral, incluso si aún no había aparecido impresa. [20] Otros han especulado que la historia de Kekulé en 1890 era una nueva parodia de la parodia del mono, y era una mera invención en lugar de un recuerdo de un evento en su vida.
El discurso de Kekulé de 1890, [21] en el que aparecen estas anécdotas, ha sido traducido al inglés. [22] Si se toma la anécdota como reflejo de un recuerdo preciso de un acontecimiento real, las circunstancias mencionadas en la historia sugieren que debe haber sucedido a principios de 1862. [23]
En el mismo discurso de 1890 contó otra anécdota autobiográfica sobre una visión anterior de átomos y moléculas danzantes que condujo a su teoría de la estructura, publicada en mayo de 1858. Esto ocurrió, según afirmó, mientras viajaba en el piso superior de un ómnibus tirado por caballos en Londres. Una vez más, si uno toma la anécdota como reflejo de un recuerdo preciso de un evento real, las circunstancias relatadas en la anécdota sugieren que debe haber ocurrido a fines del verano de 1855. [24]
Obras
- Lehrbuch der Organischen Chemie (en alemán). vol. 1. Erlangen: Enke. 1859–1861.
- Lehrbuch der Organischen Chemie (en alemán). vol. 2. Erlangen: Enke. 1862–1866.
- Lehrbuch der Organischen Chemie (en alemán). vol. 3. Erlangen: Enke. 1867.
- Lehrbuch der Organischen Chemie (en alemán). vol. 4. Stuttgart: Enke. 1880.
- Lehrbuch der Organischen Chemie (en alemán). vol. 5. Stuttgart: Enke. 1881.
- Lehrbuch der Organischen Chemie (en alemán). vol. 6. Stuttgart: Enke. 1882.
- Lehrbuch der Organischen Chemie (en alemán). vol. 7. Stuttgart: Enke. 1887.
Honores
_1964,_MiNr_440.jpg/440px-Stamps_of_Germany_(BRD)_1964,_MiNr_440.jpg)
En 1895, Kekulé fue ennoblecido por el káiser Guillermo II de Alemania , lo que le dio el derecho de añadir "von Stradonitz" a su nombre, en referencia a una posesión de sus antepasados patrilineales en Stradonice , Bohemia. Su nombre pasó a ser Friedrich August Kekule von Stradonitz, sin el acento francés en la última "e" de su nombre, y esta es la forma del nombre que utilizan algunas bibliotecas. Este título fue heredado por su hijo, el genealogista Stephan Kekule von Stradonitz . De los primeros cinco Premios Nobel de Química , tres los obtuvieron antiguos alumnos de Kekulé: van 't Hoff en 1901, Fischer en 1902 y Baeyer en 1905.
En frente del antiguo Instituto de Química (finalizado en 1868) de la Universidad de Bonn se encuentra un monumento de Kekulé de tamaño superior al natural, inaugurado en 1903. Los estudiantes suelen decorar su estatua con humor, por ejemplo, para el día de San Valentín o para Halloween .
Véase también
Referencias
- ^ "La fórmula de Kekulé". Random House Webster's Unabridged Dictionary .
- ^ Nickon, Alex; Silversmith, Ernest F. (22 de octubre de 2013). Química orgánica: el juego de los nombres: términos acuñados modernos y sus orígenes. Elsevier. ISBN 978-1-4831-4523-5.
- ^ abc Chisholm, Hugh , ed. (1911). . Encyclopædia Britannica . Vol. 15 (11.ª ed.). Cambridge University Press. págs. 717–718.
- ^ Agosto Kekulé (1857). "Über die sg gepaarten Verbindungen und die Theorie der mehratomigen Radicale". Annalen der Chemie und Pharmacie . 104 (2): 129-150. doi :10.1002/jlac.18571040202.
- ^ Agosto Kekulé (1858). "Ueber die Constitution und die Metamorphosen der chemischen Verbindungen und über die chemische Natur des Kohlenstoffs". Annalen der Chemie und Pharmacie . 106 (2): 129-159. doi :10.1002/jlac.18581060202.
- ^ COMO Couper (1858). "Sur una nouvelle théorie chimique". Annales de chimie et de physique . 53 : 488–489.
- ^ Alan J. Rocke (2010). Imagen y realidad: Kekulé, Kopp y la imaginación científica . University of Chicago Press. ISBN 978-0-226-72332-7.
- ^ "Datos históricos sobre el descubrimiento de la ley de valencia". American Journal of Mathematics . 1 (3): 282. 1878. doi :10.2307/2369316. ISSN 0002-9327. JSTOR 2369316.
- ^ Constable, Edwin C. (22 de agosto de 2019). "¿Qué hay en un nombre? Una breve historia de la química de coordinación desde entonces hasta ahora". Química 2019 . 1 (1): 126–163. doi : 10.3390/chemistry1010010 . ISSN 2624-8549.
- ^ PubChem. «Ácido peryódico». pubchem.ncbi.nlm.nih.gov . Consultado el 16 de octubre de 2024 .
- ^ Agosto Kekulé (1865). "Sur la constitución de sustancias aromáticas". Boletín de la Société Chimique de París . 3 (2): 98-110.
- ^ Agosto Kekulé (1866). "Untersuchungen úber aromatische Verbindungen". Annalen der Chemie und Pharmacie . 137 (2): 129-196. doi :10.1002/jlac.18661370202.
- ^ "Friedrich August Kekule von Stradonitz –inventor of benzene structure – World Of Chemicals". worldofchemicals.com . 28 de mayo de 2015. Archivado desde el original el 10 de noviembre de 2022 . Consultado el 2 de marzo de 2018 .
- ^ Ladenburg, Albert (1869) "Bemerkungen zur aromatischen Theorie" (Observaciones sobre la teoría aromática), Berichte der Deutschen Chemischen Gesellschaft , 2 : 140-142.
- ^ Kekulé, agosto (1872). "Ueber einige Condensationsproducte des Aldehyds (Sobre algunos productos de condensación de aldehídos)". Annalen der Chemie und Pharmacie (en alemán). 162 (2-3). Wiley: 309–320. doi :10.1002/jlac.18721620211. ISSN 0075-4617.
- ^ Pierre Laszlo (abril de 2004). "Reseña del libro: Jerome A. Berson: Chemical Discovery and the Logicians' Program. A Problematic Pairing, Wiley-VCH, Weinheim, 2003". Revista internacional de filosofía de la química . 10 (1). Hyle. ISSN 1433-5158 . Consultado el 6 de julio de 2013 .
- ^ Pauling, Linus (1 de abril de 1928). «The Shared-Electron Chemical Bond» (PDF) . Actas de la Academia Nacional de Ciencias . 14 (4): 359–362. Bibcode :1928PNAS...14..359P. doi : 10.1073/pnas.14.4.359 . PMC 1085493 . PMID 16587350. Archivado (PDF) desde el original el 11 de marzo de 2020 . Consultado el 29 de noviembre de 2020 .
- ^ Read, John (1957). De la alquimia a la química. Courier Corporation. págs. 179-180. ISBN 978-0-486-28690-7.
- ^ Traducido al inglés por D. Wilcox y F. Greenbaum, Journal of Chemical Education , 42 (1965), 266–67.
- ^ AJ Rocke (1985). "Hipótesis y experimento en la teoría del benceno de Kekulé". Anales de la ciencia . 42 (4): 355–81. doi :10.1080/00033798500200411.
- ^ Agosto Kekulé (1890). "Benzolfest: Rede". Berichte der Deutschen Chemischen Gesellschaft . 23 (1): 1302–11. doi :10.1002/cber.189002301204.
- ^ OT Benfey (1958). "August Kekulé y el nacimiento de la teoría estructural de la química orgánica en 1858". Revista de educación química . 35 (1): 21–23. Bibcode :1958JChEd..35...21B. doi :10.1021/ed035p21.
- ^ JeanGillis (1966). "Auguste Kekulé et son oeuvre, realizado en Gand de 1858 a 1867". Memorias de la Academia Real de Bélgica . 37 (1): 1–40.
- ^ Alan J. Rocke (2010). Imagen y realidad: Kekulé, Kopp y la imaginación científica . University of Chicago Press. pp. 60–66. ISBN 978-0-226-72332-7.
Lectura adicional
- Benfey, O. Theodor. "August Kekule and the Birth of the Structural Theory of Organic Chemistry in 1858" . Journal of Chemical Education . Volumen 35, N.º 1, enero de 1958. págs. 21-23. – Incluye una traducción al inglés del discurso de Kekule de 1890 en el que habló sobre su desarrollo de la teoría de la estructura y la teoría del benceno.
- Rocke, AJ, Imagen y realidad: Kekule, Kopp y la imaginación científica (University of Chicago Press, 2010).
Enlaces externos
- Kekulés Traum (El sueño de Kekulé, en alemán)
- Kekulé: un científico y un soñador
- . Nueva Enciclopedia Internacional . 1905.


