Química analítica

| Parte de una serie sobre |
| Química |
|---|
 |
La química analítica estudia y utiliza instrumentos y métodos para separar , identificar y cuantificar la materia. [1] En la práctica, la separación, identificación o cuantificación pueden constituir todo el análisis o combinarse con otro método. La separación aísla los analitos . El análisis cualitativo identifica los analitos, mientras que el análisis cuantitativo determina la cantidad numérica o concentración.
La química analítica consta de métodos químicos húmedos clásicos y técnicas analíticas modernas . [2] [3] Los métodos cualitativos clásicos utilizan separaciones como precipitación , extracción y destilación . La identificación puede basarse en diferencias de color, olor, punto de fusión, punto de ebullición, solubilidad, radiactividad o reactividad. El análisis cuantitativo clásico utiliza cambios de masa o volumen para cuantificar la cantidad. Se pueden utilizar métodos instrumentales para separar muestras mediante cromatografía , electroforesis o fraccionamiento de flujo de campo . Luego se puede realizar un análisis cualitativo y cuantitativo, a menudo con el mismo instrumento y puede utilizar interacción de luz , interacción de calor , campos eléctricos o campos magnéticos . A menudo, el mismo instrumento puede separar, identificar y cuantificar un analito.
La química analítica también se centra en las mejoras en el diseño experimental , la quimiometría y la creación de nuevas herramientas de medición. La química analítica tiene amplias aplicaciones en la medicina, la ciencia y la ingeniería.
Historia

La química analítica ha sido importante desde los inicios de la química, ya que proporciona métodos para determinar qué elementos y sustancias químicas están presentes en el objeto en cuestión. Durante este período, las contribuciones significativas a la química analítica incluyeron el desarrollo del análisis elemental sistemático por Justus von Liebig y el análisis orgánico sistematizado basado en las reacciones específicas de los grupos funcionales.
El primer análisis instrumental fue la espectrometría de emisión de llama desarrollada por Robert Bunsen y Gustav Kirchhoff, quienes descubrieron el rubidio (Rb) y el cesio (Cs) en 1860. [4]
La mayoría de los avances más importantes en química analítica tuvieron lugar después de 1900. Durante este período, el análisis instrumental se volvió cada vez más dominante en el campo. En particular, muchas de las técnicas espectroscópicas y espectrométricas básicas se descubrieron a principios del siglo XX y se perfeccionaron a fines del siglo XX. [5]
Las ciencias de separación siguen una línea temporal de desarrollo similar y también se transformaron cada vez más en instrumentos de alto rendimiento. [6] En la década de 1970, muchas de estas técnicas comenzaron a usarse juntas como técnicas híbridas para lograr una caracterización completa de las muestras.
A partir de la década de 1970, la química analítica se fue haciendo cada vez más inclusiva de cuestiones biológicas ( química bioanalítica ), mientras que anteriormente se había centrado en gran medida en moléculas inorgánicas o orgánicas pequeñas . Los láseres se han utilizado cada vez más como sondas e incluso para iniciar e influir en una amplia variedad de reacciones. A finales del siglo XX también se produjo una expansión de la aplicación de la química analítica desde cuestiones químicas algo académicas a cuestiones forenses , ambientales , industriales y médicas , como en la histología . [7]
La química analítica moderna está dominada por el análisis instrumental. Muchos químicos analíticos se centran en un solo tipo de instrumento. Los académicos tienden a centrarse en nuevas aplicaciones y descubrimientos o en nuevos métodos de análisis. El descubrimiento de una sustancia química presente en la sangre que aumenta el riesgo de cáncer sería un descubrimiento en el que podría participar un químico analítico. Un esfuerzo por desarrollar un nuevo método podría implicar el uso de un láser sintonizable para aumentar la especificidad y la sensibilidad de un método espectrométrico. Muchos métodos, una vez desarrollados, se mantienen estáticos a propósito para que los datos se puedan comparar durante largos períodos de tiempo. Esto es particularmente cierto en el control de calidad industrial (QA), las aplicaciones forenses y ambientales. La química analítica desempeña un papel cada vez más importante en la industria farmacéutica, donde, además del control de calidad, se utiliza en el descubrimiento de nuevos fármacos candidatos y en aplicaciones clínicas donde la comprensión de las interacciones entre el fármaco y el paciente es fundamental.
Métodos clásicos

Aunque la química analítica moderna está dominada por una instrumentación sofisticada, las raíces de la química analítica y algunos de los principios utilizados en los instrumentos modernos provienen de técnicas tradicionales, muchas de las cuales todavía se utilizan en la actualidad. Estas técnicas también tienden a formar la columna vertebral de la mayoría de los laboratorios educativos de química analítica de pregrado.
Análisis cualitativo
El análisis cualitativo determina la presencia o ausencia de un compuesto en particular, pero no su masa ni su concentración. Por definición, los análisis cualitativos no miden la cantidad.
Pruebas químicas
Existen numerosas pruebas químicas cualitativas, por ejemplo, la prueba del ácido para el oro y la prueba de Kastle-Meyer para la presencia de sangre .
Prueba de llama
El análisis cualitativo inorgánico generalmente se refiere a un esquema sistemático para confirmar la presencia de ciertos iones o elementos acuosos mediante la realización de una serie de reacciones que eliminan una variedad de posibilidades y luego confirman los iones sospechosos con una prueba de confirmación. A veces, en estos esquemas se incluyen pequeños iones que contienen carbono. Con la instrumentación moderna, estas pruebas rara vez se utilizan, pero pueden ser útiles para fines educativos y en el trabajo de campo u otras situaciones en las que no se dispone o no es conveniente tener acceso a instrumentos de última generación.
Análisis cuantitativo
El análisis cuantitativo es la medición de las cantidades de determinados componentes químicos presentes en una sustancia. Las cantidades se pueden medir en masa (análisis gravimétrico) o en volumen (análisis volumétrico).
Análisis gravimétrico
El análisis gravimétrico implica determinar la cantidad de material presente pesando la muestra antes y/o después de alguna transformación. Un ejemplo común utilizado en la educación universitaria es la determinación de la cantidad de agua en un hidrato calentando la muestra para eliminar el agua de modo que la diferencia de peso se deba a la pérdida de agua.
Análisis volumétrico
La titulación implica la adición gradual de un reactivo medible a un volumen exacto de una solución que se está analizando hasta que se alcanza un punto de equivalencia. La titulación es una familia de técnicas que se utilizan para determinar la concentración de un analito. [8] Titular con precisión hasta el punto de semiequivalencia o el punto final de una titulación permite al químico determinar la cantidad de moles utilizados, que luego se pueden utilizar para determinar una concentración o composición del titulante. La más familiar para aquellos que han tomado química durante la educación secundaria es la titulación ácido-base que implica un indicador que cambia de color, como la fenolftaleína . Hay muchos otros tipos de titulaciones, por ejemplo, titulaciones potenciométricas o titulaciones de precipitación. Los químicos también pueden crear curvas de titulación para probar sistemáticamente el pH de cada gota para comprender las diferentes propiedades del titulante.
Métodos instrumentales
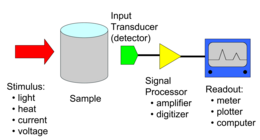
Espectroscopia
La espectroscopia mide la interacción de las moléculas con la radiación electromagnética . La espectroscopia consta de muchas aplicaciones diferentes, como la espectroscopia de absorción atómica , la espectroscopia de emisión atómica , la espectroscopia ultravioleta-visible , la espectroscopia de rayos X , la espectroscopia de fluorescencia , la espectroscopia infrarroja , la espectroscopia Raman , la interferometría de polarización dual , la espectroscopia de resonancia magnética nuclear , la espectroscopia de fotoemisión , la espectroscopia Mössbauer , etc.
Espectrometría de masas

La espectrometría de masas mide la relación masa-carga de las moléculas utilizando campos eléctricos y magnéticos . En un espectrómetro de masas, una pequeña cantidad de muestra se ioniza y se convierte en iones gaseosos, donde se separan y analizan de acuerdo con sus relaciones masa-carga . [8] Existen varios métodos de ionización: ionización electrónica , ionización química , ionización por electrospray , bombardeo rápido de átomos, desorción/ionización láser asistida por matriz y otros. Además, la espectrometría de masas se clasifica por enfoques de analizadores de masas: sector magnético , analizador de masas cuadrupolo , trampa de iones cuadrupolo , tiempo de vuelo , resonancia ciclotrónica de iones por transformada de Fourier , etc.
Análisis electroquímico
Los métodos electroanalíticos miden el potencial ( voltios ) y/o la corriente ( amperios ) en una celda electroquímica que contiene el analito. [9] [10] Estos métodos se pueden clasificar según qué aspectos de la celda se controlan y cuáles se miden. Las cuatro categorías principales son potenciometría (se mide la diferencia de potenciales de electrodos), coulometría (se mide la carga transferida a lo largo del tiempo), amperometría (se mide la corriente de la celda a lo largo del tiempo) y voltamperometría (se mide la corriente de la celda mientras se altera activamente el potencial de la celda).
La potenciometría mide el potencial de la celda, la coulometría mide la corriente de la celda y la voltamperometría mide el cambio en la corriente cuando cambia el potencial de la celda. [11] [12]
Análisis térmico
La calorimetría y el análisis termogravimétrico miden la interacción de un material y el calor .
Separación

Los procesos de separación se utilizan para reducir la complejidad de las mezclas de materiales. La cromatografía , la electroforesis y el fraccionamiento por flujo de campo son representativos de este campo.
Ensayos cromatográficos
La cromatografía se puede utilizar para determinar la presencia de sustancias en una muestra, ya que los diferentes componentes de una mezcla tienen diferentes tendencias a adsorberse en la fase estacionaria o disolverse en la fase móvil. Por lo tanto, los diferentes componentes de la mezcla se mueven a diferente velocidad. Por lo tanto, los diferentes componentes de una mezcla se pueden identificar por sus respectivos valores de R ƒ , que es la relación entre la distancia de migración de la sustancia y la distancia de migración del frente del disolvente durante la cromatografía. En combinación con los métodos instrumentales, la cromatografía se puede utilizar en la determinación cuantitativa de las sustancias. La cromatografía separa el analito del resto de la muestra para que pueda medirse sin interferencias de otros compuestos. [8] Existen diferentes tipos de cromatografía que difieren de los medios que utilizan para separar el analito y la muestra. [13] En la cromatografía de capa fina , la mezcla de analitos se mueve hacia arriba y se separa a lo largo de la lámina recubierta debajo de la fase móvil volátil. En la cromatografía de gases , el gas separa los analitos volátiles. Un método común de cromatografía que utiliza líquido como fase móvil es la cromatografía líquida de alto rendimiento .
Técnicas híbridas
Las combinaciones de las técnicas anteriores producen una técnica "híbrida" o "con guion". [14] [15] [16] [17] [18] Actualmente, se utilizan de forma popular varios ejemplos y se están desarrollando nuevas técnicas híbridas. Por ejemplo, cromatografía de gases-espectrometría de masas , cromatografía de gases - espectroscopia infrarroja , cromatografía líquida-espectrometría de masas , cromatografía líquida- espectroscopia RMN , cromatografía líquida-espectroscopia infrarroja y electroforesis capilar-espectrometría de masas.
Las técnicas de separación con guion hacen referencia a una combinación de dos (o más) técnicas para detectar y separar sustancias químicas de soluciones. La mayoría de las veces, la otra técnica es algún tipo de cromatografía . Las técnicas con guion se utilizan ampliamente en química y bioquímica . A veces se utiliza una barra en lugar de un guion , especialmente si el nombre de uno de los métodos contiene un guion.
Microscopía

La visualización de moléculas individuales, células individuales, tejidos biológicos y nanomateriales es un enfoque importante y atractivo en la ciencia analítica. Además, la hibridación con otras herramientas analíticas tradicionales está revolucionando la ciencia analítica. La microscopía se puede clasificar en tres campos diferentes: microscopía óptica , microscopía electrónica y microscopía de sonda de barrido . Recientemente, este campo está progresando rápidamente debido al rápido desarrollo de las industrias de la informática y la cámara.
Laboratorio en un chip
Dispositivos que integran (múltiples) funciones de laboratorio en un único chip de apenas milímetros a unos pocos centímetros cuadrados de tamaño y que son capaces de manejar volúmenes de fluidos extremadamente pequeños, hasta menos de picolitros.
Errores
El error puede definirse como la diferencia numérica entre el valor observado y el valor verdadero. [20] El error experimental puede dividirse en dos tipos: error sistemático y error aleatorio. El error sistemático resulta de un defecto en el equipo o en el diseño de un experimento, mientras que el error aleatorio resulta de variables no controladas o incontrolables en el experimento. [21]
En caso de error, el valor verdadero y el valor observado en el análisis químico se pueden relacionar entre sí mediante la ecuación
dónde
- es el error absoluto
- es el verdadero valor.
- es el valor observado.
Un error de una medición es una medida inversa de una medición exacta, es decir, cuanto menor sea el error mayor será la precisión de la medición.
Los errores se pueden expresar de forma relativa. Dado el error relativo( ):
El error porcentual también se puede calcular:
Si queremos utilizar estos valores en una función, también podemos querer calcular el error de la función. Sea una función con variables. Por lo tanto, se debe calcular la propagación de la incertidumbre para conocer el error en :
Normas
Curva estándar
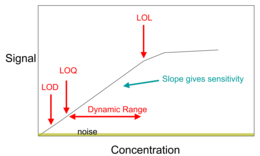
Un método general para el análisis de la concentración implica la creación de una curva de calibración . Esto permite determinar la cantidad de una sustancia química en un material comparando los resultados de una muestra desconocida con los de una serie de estándares conocidos. Si la concentración de un elemento o compuesto en una muestra es demasiado alta para el rango de detección de la técnica, simplemente se puede diluir en un disolvente puro. Si la cantidad en la muestra está por debajo del rango de medición de un instrumento, se puede utilizar el método de adición. En este método, se añade una cantidad conocida del elemento o compuesto en estudio, y la diferencia entre la concentración añadida y la concentración observada es la cantidad real en la muestra.
Normas internas
En ocasiones, se añade un estándar interno en una concentración conocida directamente a una muestra analítica para facilitar la cuantificación. Luego, se determina la cantidad de analito presente en relación con el estándar interno como calibrador. Un estándar interno ideal es un analito enriquecido isotópicamente, lo que da lugar al método de dilución isotópica .
Adición estándar
El método de adición de patrones se utiliza en el análisis instrumental para determinar la concentración de una sustancia ( analito ) en una muestra desconocida comparándola con un conjunto de muestras de concentración conocida, de forma similar al uso de una curva de calibración . La adición de patrones se puede aplicar a la mayoría de las técnicas analíticas y se utiliza en lugar de una curva de calibración para resolver el problema del efecto de la matriz .
Señales y ruido
Uno de los componentes más importantes de la química analítica es maximizar la señal deseada mientras se minimiza el ruido asociado . [22] La figura de mérito analítica se conoce como relación señal-ruido (S/N o SNR).
El ruido puede surgir de factores ambientales así como de procesos físicos fundamentales.
Ruido térmico
El ruido térmico es el resultado del movimiento de los portadores de carga (normalmente electrones) en un circuito eléctrico generado por su movimiento térmico. El ruido térmico es ruido blanco, lo que significa que la densidad espectral de potencia es constante en todo el espectro de frecuencias .
El valor cuadrático medio del ruido térmico en una resistencia se da por [22]
donde k B es la constante de Boltzmann , T es la temperatura , R es la resistencia y es el ancho de banda de la frecuencia .
Ruido de disparo
El ruido de disparo es un tipo de ruido electrónico que se produce cuando el número finito de partículas (como electrones en un circuito electrónico o fotones en un dispositivo óptico) es lo suficientemente pequeño como para dar lugar a fluctuaciones estadísticas en una señal.
El ruido de disparo es un proceso de Poisson y los portadores de carga que forman la corriente siguen una distribución de Poisson . La fluctuación de la corriente cuadrática media se da por [22]
donde e es la carga elemental e I es la corriente media. El ruido de disparo es ruido blanco.
Ruido de parpadeo
El ruido de parpadeo es un ruido electrónico con un espectro de frecuencia 1/ ƒ ; a medida que f aumenta, el ruido disminuye. El ruido de parpadeo surge de una variedad de fuentes, como impurezas en un canal conductor, ruido de generación y recombinación en un transistor debido a la corriente de base, etc. Este ruido se puede evitar mediante la modulación de la señal a una frecuencia más alta, por ejemplo, mediante el uso de un amplificador lock-in .
Ruido ambiental
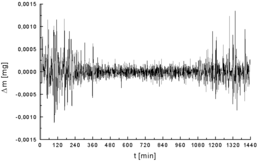
El ruido ambiental surge de los alrededores del instrumento analítico. Las fuentes de ruido electromagnético son las líneas eléctricas , las estaciones de radio y televisión, los dispositivos inalámbricos , las lámparas fluorescentes compactas [23] y los motores eléctricos . Muchas de estas fuentes de ruido tienen un ancho de banda estrecho y, por lo tanto, se pueden evitar. Es posible que se requiera aislamiento de temperatura y vibración para algunos instrumentos.
Reducción de ruido
La reducción de ruido se puede lograr tanto en hardware como en software . Algunos ejemplos de reducción de ruido de hardware son el uso de cable blindado , filtrado analógico y modulación de señal. Algunos ejemplos de reducción de ruido de software son el filtrado digital , el promedio de conjunto , el promedio de boxcar y los métodos de correlación . [22]
Aplicaciones
_(8225044148).jpg/440px-Portable_Screening_Devices_(1435)_(8225044148).jpg)
La química analítica tiene aplicaciones que incluyen la ciencia forense , el bioanálisis , el análisis clínico , el análisis ambiental y el análisis de materiales . La investigación en química analítica está impulsada en gran medida por el rendimiento (sensibilidad, límite de detección , selectividad, robustez, rango dinámico , rango lineal , exactitud, precisión y velocidad) y el costo (compra, operación, capacitación, tiempo y espacio). Entre las principales ramas de la espectrometría atómica analítica contemporánea, las más extendidas y universales son la espectrometría óptica y de masas. [24] En el análisis elemental directo de muestras sólidas, los nuevos líderes son la descomposición inducida por láser y la espectrometría de masas por ablación láser , y las técnicas relacionadas con la transferencia de los productos de ablación láser a plasma acoplado inductivamente . Los avances en el diseño de láseres de diodo y osciladores paramétricos ópticos promueven desarrollos en espectrometría de fluorescencia e ionización y también en técnicas de absorción donde se espera que se expandan los usos de cavidades ópticas para una mayor longitud de trayectoria de absorción efectiva. El uso de métodos basados en plasma y láser está aumentando. Se ha reactivado el interés por el análisis absoluto (sin estándares), en particular en la espectrometría de emisión. [ cita requerida ]
Se están haciendo grandes esfuerzos para reducir las técnicas de análisis al tamaño de un chip . Aunque hay pocos ejemplos de sistemas de este tipo que compitan con las técnicas de análisis tradicionales, las posibles ventajas incluyen tamaño/portabilidad, velocidad y costo ( sistema de análisis total micro (μTAS) o laboratorio en un chip ). La química a microescala reduce las cantidades de sustancias químicas utilizadas.
Muchos avances mejoran el análisis de los sistemas biológicos. Ejemplos de campos en rápida expansión en esta área son la genómica , la secuenciación de ADN y la investigación relacionada con la huella genética y la micromatriz de ADN ; la proteómica , el análisis de las concentraciones y modificaciones de proteínas, especialmente en respuesta a diversos factores estresantes, en diversas etapas del desarrollo o en diversas partes del cuerpo ; la metabolómica , que se ocupa de los metabolitos; la transcriptómica , que incluye el ARNm y los campos asociados; la lipidómica , que trata de los lípidos y sus campos asociados; la peptidómica, que trata de los péptidos y sus campos asociados; y la metalómica, que trata de las concentraciones de metales y especialmente de su unión a las proteínas y otras moléculas. [ cita requerida ]
La química analítica ha desempeñado un papel fundamental en la comprensión de la ciencia básica para una variedad de aplicaciones prácticas, como aplicaciones biomédicas, monitoreo ambiental , control de calidad de la fabricación industrial, ciencia forense, etc. [25]
Los recientes avances en automatización informática y tecnologías de la información han extendido la química analítica a una serie de nuevos campos biológicos. Por ejemplo, las máquinas de secuenciación automática de ADN fueron la base para completar proyectos sobre el genoma humano que condujeron al nacimiento de la genómica . La identificación de proteínas y la secuenciación de péptidos mediante espectrometría de masas abrieron un nuevo campo de la proteómica . Además de automatizar procesos específicos, se están realizando esfuerzos para automatizar secciones más grandes de pruebas de laboratorio, como en empresas como Emerald Cloud Lab y Transcriptic. [26]
La química analítica ha sido un área indispensable en el desarrollo de la nanotecnología . Los instrumentos de caracterización de superficies, los microscopios electrónicos y los microscopios de sonda de barrido permiten a los científicos visualizar estructuras atómicas con caracterizaciones químicas.
Véase también
- Calorímetro
- Química clínica
- Análisis de haz de iones
- Lista de métodos de análisis químico
- Publicaciones importantes en química analítica
- Lista de métodos de análisis de materiales
- Incertidumbre de medición
- Metrología
- Microanálisis
- Análisis de la reacción nuclear
- Calidad de los resultados analíticos
- Química radioanalítica
- Espectroscopia de retrodispersión de Rutherford
- Análisis sensorial en el campo de la ciencia de los alimentos
- Instrumentación virtual
- Rango de trabajo
Referencias
- ^ Skoog, Douglas A.; West, Donald M.; Holler, F. James; Crouch, Stanley R. (2014). Fundamentos de química analítica . Belmont: Brooks/Cole, Cengage Learning. pág. 1. ISBN 978-0-495-55832-3.
- ^ Skoog, Douglas A.; Holler, F. James; Crouch, Stanley R. (2007). Principios del análisis instrumental . Belmont, CA: Brooks/Cole, Thomson. pág. 1. ISBN 978-0-495-01201-6.
- ^ "Técnica analítica". Archivado desde el original el 17 de marzo de 2013. Consultado el 17 de enero de 2013 .
- ^ Arikawa, Yoshiko (2001). "Basic Education in Analytical Chemistry" (pdf) . Analytical Sciences . 17 (Suplemento): i571–i573 . Consultado el 10 de enero de 2014 .
- ^ Miller, K; Synovec, RE (2000). "Revisión de mediciones analíticas facilitadas por la tecnología de formación de gotas". Talanta . 51 (5): 921–33. doi :10.1016/S0039-9140(99)00358-6. PMID 18967924.
- ^ Bartle, Keith D.; Myers, Peter (2002). "Historia de la cromatografía de gases". TrAC Trends in Analytical Chemistry . 21 (9–10): 547. doi :10.1016/S0165-9936(02)00806-3.
- ^ Laitinen, HA (1989). "Historia de la química analítica en Estados Unidos". Talanta . 36 (1–2): 1–9. doi :10.1016/0039-9140(89)80077-3. PMID 18964671.
- ^ abc Douglas A. Skoog; Stanley R. Crouch (2014). Fundamentos de química analítica (novena edición). Belmont, CA. ISBN 978-0-495-55828-6.OCLC 824171785 .
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) - ^ Bard, Allen J.; Faulkner, Larry R. (2000). Métodos electroquímicos: fundamentos y aplicaciones (2.ª ed.). Nueva York: John Wiley & Sons. ISBN 0-471-04372-9.[ página necesaria ]
- ^ Skoog, Douglas A.; West, Donald M.; Holler, F. James (1988). Fundamentos de química analítica (quinta edición). Nueva York: Saunders College Publishing. ISBN 0030148286.[ página necesaria ]
- ^ Skoog, Douglas A.; Donald M. West; F. James Holler (1996). Fundamentos de química analítica (7.ª ed.). Fort Worth: Saunders College Pub. ISBN 0-03-005938-0.OCLC 33112372 .
- ^ Bard, Allen J.; Larry R. Faulkner (2001). Métodos electroquímicos: fundamentos y aplicaciones (segunda edición). Hoboken, NJ. ISBN 0-471-04372-9.OCLC 43859504 .
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) - ^ Poole, CF (1 de enero de 2000), "CROMATOGRAFÍA", en Wilson, Ian D. (ed.), Enciclopedia de la ciencia de la separación , Oxford: Academic Press, págs. 40-64, ISBN 978-0-12-226770-3, consultado el 7 de octubre de 2022
- ^ Wilkins, C. (1983). "Técnicas con guiones para el análisis de mezclas orgánicas complejas". Science . 222 (4621): 291–6. Bibcode :1983Sci...222..291W. doi :10.1126/science.6353577. PMID 6353577.
- ^ Holt, RM; Newman, MJ; Pullen, FS; Richards, DS; Swanson, AG (1997). "Cromatografía líquida de alto rendimiento/espectrometría RMN/espectrometría de masas: nuevos avances en tecnología con guiones". Journal of Mass Spectrometry . 32 (1): 64–70. Bibcode :1997JMSp...32...64H. doi :10.1002/(SICI)1096-9888(199701)32:1<64::AID-JMS450>3.0.CO;2-7. PMID 9008869.
- ^ Ellis, Lyndon A; Roberts, David J (1997). "Métodos cromatográficos y con guiones para el análisis de especiación elemental en medios ambientales". Journal of Chromatography A . 774 (1–2): 3–19. doi :10.1016/S0021-9673(97)00325-7. PMID 9253184.
- ^ Guetens, G; De Boeck, G; Madera, M; Maes, RAA; Eggermont, AAM; Highley, MS; Van Oosterom, AT; De Bruijn, EA; Tjaden, UR (2002). "Técnicas con guiones en el seguimiento de fármacos contra el cáncer". Revista de cromatografía A. 976 (1–2): 229–38. doi :10.1016/S0021-9673(02)01228-1. PMID 12462614.
- ^ Guetens, G; De Boeck, G; Highley, MS; Madera, M; Maes, RAA; Eggermont, AAM; Hanauske, A; De Bruijn, EA; Tjaden, UR (2002). "Técnicas con guiones en el seguimiento de fármacos contra el cáncer". Revista de cromatografía A. 976 (1–2): 239–47. doi :10.1016/S0021-9673(02)01227-X. PMID 12462615.
- ^ Schermelleh, L.; Carlton, PM; Haase, S.; Shao, L.; Winoto, L.; Kner, P.; Burke, B.; Cardoso, MC; Agard, DA; Gustafsson, MGL; Leonhardt, H.; Sedat, JW (2008). "Imágenes multicolores de subdifracción de la periferia nuclear con microscopía de iluminación estructurada 3D". Science . 320 (5881): 1332–6. Bibcode :2008Sci...320.1332S. doi :10.1126/science.1156947. PMC 2916659 . PMID 18535242.
- ^ GL David - Química Analítica
- ^ Harris, Daniel C.; Lucy, Charles A. (29 de mayo de 2015). Análisis químico cuantitativo (novena edición). Nueva York. ISBN 978-1-4641-3538-5.OCLC 915084423 .
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) - ^ abcd Crouch, Stanley; Skoog, Douglas A. (2007). Principios del análisis instrumental . Australia: Thomson Brooks/Cole. ISBN 978-0-495-01201-6.[ página necesaria ]
- ^ "Preocupaciones sanitarias asociadas con la iluminación energéticamente eficiente y sus emisiones electromagnéticas" (PDF) . Universidad de Trent, Peterborough, ON, Canadá. Archivado (PDF) desde el original el 2022-10-09 . Consultado el 2011-11-12 .
- ^ Bol'Shakov, Aleksandr A; Ganeev, Aleksandr A; Nemets, Valerii M (2006). "Perspectivas en espectrometría atómica analítica". Russian Chemical Reviews . 75 (4): 289. arXiv : physics/0607078 . Código Bibliográfico :2006RuCRv..75..289B. doi :10.1070/RC2006v075n04ABEH001174. S2CID 95353695.
- ^ "Química analítica - Sociedad Química Estadounidense". Sociedad Química Estadounidense . Consultado el 26 de mayo de 2017 .
- ^ Groth, P.; Cox, J. (2017). "Indicadores para el uso de laboratorios robóticos en investigación biomédica básica: un análisis de la literatura". PeerJ . 5 : e3997. doi : 10.7717/peerj.3997 . PMC 5681851 . PMID 29134146.
Lectura adicional
- Gurdeep, Chatwal Anand (2008). Métodos instrumentales de análisis químico Himalaya Publishing House (India) ISBN 978-81-8318-802-9
- Ralph L. Shriner, Reynold C. Fuson, David Y. Curtin, Terence C. Morill: La identificación sistemática de compuestos orgánicos - un manual de laboratorio , Verlag Wiley, Nueva York 1980, 6.ª edición, ISBN 0-471-78874-0 .
- Bettencourt da Silva, R; Bulska, E; Godlewska-Zylkiewicz, B; Hedrich, M; Majcen, N; Magnusson, B; Marincic, S; Papadakis, I; Patriarca, M; Vassileva, E; Taylor, P; Medición analítica: incertidumbre de medición y estadísticas, 2012, ISBN 978-92-79-23071-4 .
Enlaces externos
- Infografía y animación que muestra el progreso de la química analítica.
- Espectrofotómetro de absorción atómica aas















